Secțiuni de site
Alegerea editorului:
- Structura Ministerului Apărării, revizuire militară, Ministerul Apărării, arme, știri militare, ordine ale Ministerului Apărării, armata rusă, forțe armate, marina, aviație, ofițeri, ordine ale președintelui Federației Ruse, marine, rusă Armata, Forțele Aeriene, Marină
- Unde au loc cel mai des cutremure?
- Engleza de la zero: cum să începeți să învățați cu succes
- Copiii se gătesc singuri: rețete simple ilustrate
- Ce poți găti pentru un copil de 2 ani?
- Analiza gramaticală a propozițiilor în limba rusă: exemple
- Care sunt simptomele și tratamentul orhitei cauzele orhitei
- Căderea lui Tobruk Secțiunile acestei pagini
- Diabetul insipid, ce este?
- Horoscopul Capricornului pietre talismane după data nașterii
Publicitate
| Elemente din primul grup al tabelului periodic. Istoria creației și dezvoltării |
|
Secolul al XIX-lea din istoria omenirii este un secol în care au fost reformate multe științe, inclusiv chimia. În acest moment a apărut sistemul periodic al lui Mendeleev și, odată cu acesta, legea periodică. El a devenit baza chimiei moderne. Sistemul periodic al lui D.I Mendeleev este o sistematizare a elementelor care stabilește dependența proprietăților chimice și fizice de structura și sarcina atomului unei substanțe. PovesteÎnceputul perioadei periodice a fost stabilit de cartea „Corelarea proprietăților cu greutatea atomică a elementelor”, scrisă în al treilea sfert al secolului al XVII-lea. A afișat conceptele de bază ale elementelor chimice cunoscute (la acea vreme erau doar 63 dintre ele). În plus, masele atomice ale multora dintre ele au fost determinate incorect. Acest lucru a interferat foarte mult cu descoperirea lui D.I Mendeleev. Dmitri Ivanovici și-a început munca comparând proprietățile elementelor. În primul rând, a lucrat la clor și potasiu și abia apoi a trecut la lucrul cu metale alcaline. Înarmat cu carduri speciale pe care erau înfățișate elemente chimice, el a încercat în mod repetat să asambleze acest „mozaic”: l-a așezat pe masa sa în căutarea combinațiilor și a potrivirilor necesare. După mult efort, Dmitri Ivanovici a găsit în sfârșit modelul pe care îl căuta și a aranjat elementele în rânduri periodice. După ce a primit ca rezultat celule goale între elemente, omul de știință și-a dat seama că nu toate elementele chimice erau cunoscute de cercetătorii ruși și că el era cel care trebuie să ofere acestei lumi cunoștințele în domeniul chimiei care nu fuseseră încă date de către el. predecesorii.
Toată lumea știe mitul că tabelul periodic i-a apărut lui Mendeleev într-un vis și el a adunat elementele într-un singur sistem din memorie. Aceasta este, în linii mari, o minciună. Faptul este că Dmitri Ivanovici a lucrat destul de mult și s-a concentrat pe munca sa și l-a epuizat foarte mult. În timp ce lucra la sistemul de elemente, Mendeleev a adormit odată. Când s-a trezit, și-a dat seama că nu terminase masa și mai degrabă a continuat să umple celulele goale. Cunoscutul său, un anume Inostrantsev, profesor universitar, a decis că tabelul periodic a fost visat de Mendeleev și a răspândit acest zvon printre studenții săi. Așa a apărut această ipoteză. FaimaElementele chimice ale lui Mendeleev sunt o reflectare a legii periodice create de Dmitri Ivanovici în al treilea sfert al secolului al XIX-lea (1869). În 1869, notificarea lui Mendeleev despre crearea unei anumite structuri a fost citită la o întâlnire a comunității chimice ruse. Și în același an, a fost publicată cartea „Fundamentals of Chemistry”, în care a fost publicat pentru prima dată sistemul periodic de elemente chimice al lui Mendeleev. Și în cartea „Sistemul natural al elementelor și utilizarea sa pentru a indica calitățile elementelor nedescoperite”, D. I. Mendeleev a menționat pentru prima dată conceptul de „lege periodică”.
Structura si regulile de amplasare a elementelorPrimii pași în crearea legii periodice au fost făcuți de Dmitri Ivanovici încă din anii 1869-1871, la vremea aceea a muncit din greu pentru a stabili dependența proprietăților acestor elemente de masa atomului lor. Versiunea modernă constă din elemente rezumate într-un tabel bidimensional. Poziția unui element în tabel poartă o anumită semnificație chimică și fizică. Prin locația unui element în tabel, puteți afla care este valența acestuia și puteți determina alte caracteristici chimice. Dmitri Ivanovici a încercat să stabilească o legătură între elemente, atât similare ca proprietăți, cât și diferite.
El a bazat clasificarea elementelor chimice cunoscute la acea vreme pe valență și masa atomică. Comparând proprietățile relative ale elementelor, Mendeleev a încercat să găsească un model care să unească toate elementele chimice cunoscute într-un singur sistem. Aranjandu-le pe baza maselor atomice in crestere, el a obtinut inca periodicitate in fiecare dintre randuri. Dezvoltarea în continuare a sistemuluiTabelul periodic, care a apărut în 1969, a fost rafinat de mai multe ori. Odată cu apariția gazelor nobile în anii 1930, a fost posibil să se dezvăluie o nouă dependență a elementelor - nu de masă, ci de numărul atomic. Mai târziu, a fost posibil să se stabilească numărul de protoni din nucleele atomice și s-a dovedit că acesta coincide cu numărul atomic al elementului. Oamenii de știință din secolul al XX-lea au studiat energia electronică. S-a dovedit că afectează și periodicitatea. Acest lucru a schimbat foarte mult ideile despre proprietățile elementelor. Acest punct a fost reflectat în edițiile ulterioare ale tabelului periodic al lui Mendeleev. Fiecare nouă descoperire a proprietăților și caracteristicilor elementelor se încadrează organic în tabel. Caracteristicile sistemului periodic lui MendeleevTabelul periodic este împărțit în perioade (7 rânduri dispuse orizontal), care, la rândul lor, sunt împărțite în mari și mici. Perioada începe cu un metal alcalin și se termină cu un element cu proprietăți nemetalice.
În ciuda corectitudinii și acurateții sistemului periodic, comunitatea științifică nu a vrut să recunoască această descoperire de mult timp. Mulți mari oameni de știință au ridiculizat munca lui D.I Mendeleev și au crezut că este imposibil de prezis proprietățile unui element care nu fusese încă descoperit. Dar după ce au fost descoperite presupusele elemente chimice (și acestea erau, de exemplu, scandiu, galiu și germaniu), sistemul Mendeleev și legea lui periodică au devenit știința chimiei. Masa în timpurile moderneTabelul periodic al elementelor lui Mendeleev stă la baza majorității descoperirilor chimice și fizice legate de știința atomo-moleculară. Conceptul modern de element a fost format tocmai datorită marelui om de știință. Apariția sistemului periodic al lui Mendeleev a introdus schimbări fundamentale în înțelegerea diferiților compuși și substanțe simple. Crearea tabelului periodic de către oamenii de știință a avut un impact uriaș asupra dezvoltării chimiei și a tuturor științelor legate de aceasta. Tabelul periodic este una dintre cele mai mari descoperiri ale omenirii, care a făcut posibilă organizarea cunoștințelor despre lumea din jurul nostru și descoperirea elemente chimice noi. Este necesar pentru școlari, precum și pentru oricine este interesat de chimie. În plus, această schemă este indispensabilă în alte domenii ale științei. Această schemă conține toate elementele cunoscute de om și sunt grupate în funcție de masa atomică și numărul atomic. Aceste caracteristici afectează proprietățile elementelor. În total, sunt 8 grupuri în versiunea scurtă a tabelului, elementele incluse într-un grup au proprietăți foarte asemănătoare. Primul grup conține hidrogen, litiu, potasiu, cupru, a căror pronunție latină în rusă este cuprum. Și, de asemenea, argentum - argint, cesiu, aur - aurum și franciu. Al doilea grup conține beriliu, magneziu, calciu, zinc, urmat de stronțiu, cadmiu, bariu, iar grupul se termină cu mercur și radiu. În a șaptea grupă, primul element este fluorul, urmat de clor, mangan, brom, tehnețiu, urmat de iod, apoi reniu, astatin și bohrium. Ultimul grup este cele mai numeroase. Include gaze precum heliu, neon, argon, cripton, xenon și radon. Acest grup include și metale fier, cobalt, nichel, rodiu, paladiu, ruteniu, osmiu, iridiu și platină. Urmează hannium și meitnerium. Elementele care formează seria actinidelor și seria lantanidelor. Au proprietăți similare cu lantanul și actiniul.
Această schemă include toate tipurile de elemente, care sunt împărțite în 2 grupuri mari - metale și nemetale, având proprietăți diferite. Modul de a determina dacă un element aparține unui grup sau altuia va fi ajutat de o linie convențională care trebuie trasă de la bor la astatin. Trebuie amintit că o astfel de linie poate fi trasă numai în versiunea completă a tabelului. Toate elementele care se află deasupra acestei linii și sunt situate în subgrupele principale sunt considerate nemetale. Iar cele de mai jos, în principalele subgrupe, sunt metale. Metalele sunt, de asemenea, substanțe găsite în subgrupuri laterale. Există imagini și fotografii speciale în care vă puteți familiariza în detaliu cu poziția acestor elemente. Este demn de remarcat faptul că acele elemente care se află pe această linie prezintă aceleași proprietăți atât ale metalelor, cât și ale nemetalelor. O listă separată este alcătuită din elemente amfotere, care au proprietăți duble și pot forma 2 tipuri de compuși în urma reacțiilor. În același timp, se manifestă atât de bază, cât și proprietăți acide. Predominanța anumitor proprietăți depinde de condițiile de reacție și de substanțele cu care reacționează elementul amfoter.
Este de remarcat faptul că această schemă, în designul său tradițional de bună calitate, este colorată. În același timp, pentru ușurința orientării, acestea sunt indicate în culori diferite. subgrupe principale și secundare. Elementele sunt, de asemenea, grupate în funcție de asemănarea proprietăților lor.
Examenul de stat unificat de astăzi este principalul tip de test de la sfârșitul școlii, ceea ce înseamnă că trebuie acordată o atenție deosebită pregătirii pentru acesta. Prin urmare, atunci când alegeți examen final la chimie, trebuie să fii atent la materialele care te pot ajuta să-l treci. De regulă, școlarilor li se permite să folosească unele tabele în timpul examenului, în special, tabelul periodic de bună calitate. Prin urmare, pentru ca acesta să aducă numai beneficii în timpul testării, trebuie acordată atenție în prealabil structurii sale și studiului proprietăților elementelor, precum și secvenței acestora. De asemenea, trebuie să înveți utilizați versiunea alb-negru a tabelului pentru a nu întâmpina unele dificultăţi la examen.
Pe lângă tabelul principal care caracterizează proprietățile elementelor și dependența lor de masa atomică, există și alte diagrame care pot ajuta la studiul chimiei. De exemplu, există tabele de solubilitate și electronegativitate a substanțelor. Primul poate fi folosit pentru a determina cât de solubil este un anumit compus în apă la temperatură normală. În acest caz, anionii sunt localizați orizontal - ionii încărcați negativ, iar cationii - adică ionii încărcați pozitiv - sunt localizați vertical. Pentru a afla gradul de solubilitate a unuia sau altui compus, este necesar să găsiți componentele acestuia folosind tabelul. Și la locul intersecției lor va exista desemnarea necesară. Dacă este litera „p”, atunci substanța este complet solubilă în apă în condiții normale. Dacă litera „m” este prezentă, substanța este ușor solubilă, iar dacă litera „n” este prezentă, este aproape insolubilă. Dacă există semnul „+”, compusul nu formează un precipitat și reacționează cu solventul fără reziduuri. Dacă este prezent un semn „-”, înseamnă că o astfel de substanță nu există. Uneori puteți vedea și semnul „?” în tabel, atunci aceasta înseamnă că gradul de solubilitate al acestui compus nu este cunoscut cu siguranță. Electronegativitatea elementelor poate varia de la 1 la 8 există și un tabel special pentru a determina acest parametru.
Imagini din tabelul periodic de bună calitateAceastă schemă este una dintre cele mai mari realizări în domeniul chimiei. În același timp există multe tipuri de acest tabel– versiune scurtă, lungă, precum și extra-lungă. Cel mai comun este tabelul scurt, dar varianta lungă a diagramei este și ea comună. Este de remarcat faptul că versiunea scurtă a circuitului nu este recomandată în prezent pentru utilizare de către IUPAC. TABELUL PERIODIC LUI MENDELEEV Construcția tabelului periodic al elementelor chimice a lui Mendeleev corespunde perioadelor caracteristice teoriei numerelor și bazelor ortogonale. Adăugarea matricelor Hadamard cu matrici de ordine pare și impar creează o bază structurală a elementelor matricei imbricate: matrice de ordinea întâi (Odin), a doua (Euler), a treia (Mersenne), a patra (Hadamard) și a cincea (Fermat). Este ușor de observat că sunt 4 comenzi k Matricele Hadamard corespund elementelor inerte cu o masă atomică multiplu de patru: heliu 4, neon 20, argon 40 (39.948), etc., dar și elementele de bază ale vieții și tehnologiei digitale: carbon 12, oxigen 16, siliciu 28 , germaniu 72. Se pare că cu matrice Mersenne de ordine 4 k–1, dimpotrivă, tot ce este activ, otrăvitor, distructiv și coroziv este legat. Dar acestea sunt și elemente radioactive - surse de energie și plumb 207 (produsul final, sărurile otrăvitoare). Fluorul, desigur, este 19. Ordinele matricelor Mersenne corespund secvenței elementelor radioactive numite seria actiniului: uraniu 235, plutoniu 239 (un izotop care este o sursă mai puternică de energie atomică decât uraniul) etc. Acestea sunt, de asemenea, metale alcaline litiu 7, sodiu 23 și potasiu 39.
Galiu – greutate atomică 68 comenzi 4 k–2 Matrice Euler (Mersenne dublă) corespund azotului 14 (baza atmosferei). Sarea de masă este formată din doi atomi de sodiu 23 și clor 35 „cum ar fi mersenne”, această combinație este caracteristică matricelor Euler. Clorul mai masiv, cu o greutate de 35,4, este puțin sub dimensiunea Hadamard de 36. Cristale de sare de masă: un cub (! adică un personaj docil, Hadamards) și un octaedru (mai sfidător, acesta este, fără îndoială, Euler). În fizica atomică, tranziția fier 56 - nichel 59 este granița dintre elementele care furnizează energie în timpul sintezei unui nucleu mai mare (bombă cu hidrogen) și dezintegrare (bombă cu uraniu). Ordinul 58 este renumit pentru faptul că nu numai că nu există analogi ai matricelor Hadamard sub forma matricelor Belevich cu zerouri pe diagonală, ci și nu există multe matrici ponderate pentru el - cel mai apropiat ortogonal W(58,53) are 5 zerouri în fiecare coloană și rând (decalaj adânc). În seria corespunzătoare matricelor Fermat și substituțiilor lor de ordinul 4 k+1, prin voința sorții costă Fermium 257. Nu poți spune nimic, o lovitură exactă. Aici există aurul 197. Cuprul 64 (63.547) și argintul 108 (107.868), simboluri ale electronicii, nu ajung, după cum se vede, la aur și corespund unor matrici Hadamard mai modeste. Cuprul, cu greutatea sa atomică nu departe de 63, este activ din punct de vedere chimic - oxizii săi verzi sunt bine cunoscuți.
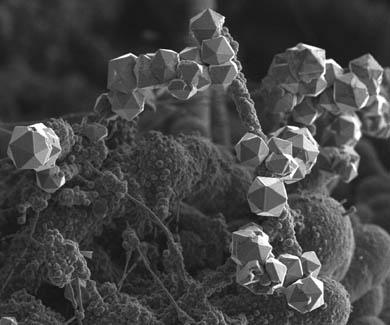
Cristale de bor sub mărire mare CU raportul de aur borul este legat - masa atomică dintre toate celelalte elemente este cea mai apropiată de 10 (mai precis 10,8, proximitatea greutății atomice de numerele impare are și un efect). Borul este un element destul de complex. Borul joacă un rol complicat în istoria vieții însăși. Structura cadrului în structurile sale este mult mai complexă decât în diamant. Tipul unic de legătură chimică care permite borului să absoarbă orice impuritate este foarte puțin înțeles, deși un număr mare de oameni de știință au primit deja premii Nobel pentru cercetările legate de acesta. Forma cristalului de bor este un icosaedru, cu cinci triunghiuri formând vârful. Misterul Platinei. Cel de-al cincilea element este, fără îndoială, metalele nobile precum aurul. Suprastructură peste dimensiunea 4 Hadamard k, 1 mare.
Uraniu izotop stabil 238 Să ne amintim, totuși, că numerele Fermat sunt rare (cel mai apropiat este 257). Cristalele de aur nativ au o formă apropiată de cub, dar și pentagrama strălucește. Cel mai apropiat vecin al său, platina, un metal nobil, se află la mai puțin de 4 greutate atomică distanță de aurul 197. Platina are o greutate atomică nu de 193, dar puțin mai mare, 194 (ordinea matricelor Euler). Este un lucru mic, dar o aduce în tabăra elementelor ceva mai agresive. Merită să ne amintim, în legătură, că, datorită inerției sale (se dizolvă, poate, în acva regia), platina este folosită ca catalizator activ pentru procesele chimice. Platina spongioasă aprinde hidrogenul la temperatura camerei. Caracterul lui Platinum nu este deloc pașnic; iridium 192 (un amestec de izotopi 191 și 193) se comportă mai pașnic. Seamănă mai mult cu cuprul, dar cu greutatea și caracterul aurului. Între neon 20 și sodiu 23 nu există niciun element cu greutatea atomică 22. Desigur, greutățile atomice sunt o caracteristică integrală. Dar printre izotopi, la rândul lor, există și o corelație interesantă a proprietăților cu proprietățile numerelor și matricele corespunzătoare ale bazelor ortogonale. Combustibilul nuclear cel mai utilizat este izotopul uraniului 235 (ordinea matricei Mersenne), în care este posibilă o reacție nucleară în lanț autosusținută. În natură, acest element apare sub formă stabilă de uraniu 238 (ordinul matricei euleriane). Nu există niciun element cu greutatea atomică 13. În ceea ce privește haosul, se corelează numărul limitat de elemente stabile ale tabelului periodic și dificultatea de a găsi matrici de nivel de ordin înalt din cauza barierei observate în matricele de ordinul al treisprezecelea.
Izotopi ai elementelor chimice, insula de stabilitate Eter în tabelul periodic Eterul lumii este substanța FIECĂRUI element chimic și, prin urmare, FIECARE substanță este adevărata materie Absolută ca Esență formatoare de element universal.Eterul mondial este sursa și coroana întregului tabel periodic autentic, începutul și sfârșitul său - alfa și omega din Tabelul periodic al elementelor lui Dmitri Ivanovici Mendeleev. În filosofia antică, eterul (aithér-greacă), alături de pământ, apă, aer și foc, este unul dintre cele cinci elemente ale ființei (după Aristotel) - a cincea esență (quinta essentia - latină), înțeleasă ca cea mai fină materie atotpătrunzătoare. La sfârșitul secolului al XIX-lea, ipoteza unui eter mondial (ME) care umple tot spațiul lumii a fost răspândită pe scară largă în cercurile științifice. A fost înțeles ca un lichid fără greutate și elastic care pătrunde în toate corpurile. Ei au încercat să explice multe fenomene și proprietăți fizice prin existența eterului. Prefaţă. Mendeleev a avut două descoperiri științifice fundamentale: 1 - Descoperirea legii periodice în substanța chimiei, 2 - Descoperirea relației dintre substanța chimiei și substanța eterului și anume: particulele de eter formează molecule, nuclei, electroni etc., dar nu participă la reacții chimice. Eterul este particule de materie ~ 10-100 de metri în dimensiune (de fapt, ele sunt „primele cărămizi” ale materiei). Fapte. Eterul era în tabelul periodic original. Celula pentru Eter a fost situată în grupul zero cu gaze inerte și în rândul zero ca principal factor de formare a sistemului pentru construirea Sistemului de elemente chimice. După moartea lui Mendeleev, tabelul a fost distorsionat prin eliminarea Eterului din el și eliminarea grupului zero, ascunzând astfel descoperirea fundamentală a semnificației conceptuale. Un astfel de fals intenționat împiedică dezvoltarea progresului civilizației. Rezultat. În școli și universități predau un tabel periodic decupat. Concluzie. Revenirea la adevăratul tabel periodic nu mai este o întrebare științifică, ci o problemă politică.
Care a fost principala semnificație politică a învățăturii lui Einstein? A constat în întreruperea accesului omenirii la sursele naturale inepuizabile de energie prin orice mijloace, care au fost deschise prin studiul proprietăților eterului mondial. Dacă reușește pe această cale, oligarhia financiară globală și-ar pierde puterea în această lume, mai ales în lumina retrospectivei acelor ani: Rockefeller au făcut o avere de neimaginat, depășind bugetul Statelor Unite, pe speculația petrolului și pierderea. a rolului petrolului pe care l-a ocupat „aurul negru” în această lume – rolul sânului vital al economiei globale – nu i-a inspirat. Acest lucru nu a inspirat alți oligarhi - regii cărbunelui și oțelului. Astfel, magnatul financiar Morgan a încetat imediat să finanțeze experimentele lui Nikola Tesla când s-a apropiat de transferul de energie fără fir și de a extrage energie „din neant” - din eterul lumii. După aceea, nimeni nu a oferit asistență financiară proprietarului unui număr imens de soluții tehnice puse în practică - solidaritatea magnaților financiari este ca cea a hoților în drept și un nas fenomenal de unde vine pericolul. De aceea împotriva umanității și a fost efectuat un sabotaj sub denumirea de „Teoria specială a relativității”. Una dintre primele lovituri a venit la tabelul lui Dmitri Mendeleev, în care eterul a fost primul număr, au fost gândurile despre eter care au dat naștere strălucirii lui Mendeleev - tabelul său periodic al elementelor.
Capitolul din articol: V.G. Rodionov. Locul și rolul eterului mondial în adevărata masă a D.I. Mendeleev 6. Argumentum ad rem Ceea ce este prezentat acum în școli și universități sub titlul „Tabel periodic al elementelor chimice D.I. Mendeleev,” este o falsitate totală. Ultima dată când Tabelul periodic real a fost publicat într-o formă nedistorsionată a fost în 1906 la Sankt Petersburg (manual „Fundamentals of Chemistry”, ediția a VIII-a). Și numai după 96 de ani de uitare, Tabelul periodic original se ridică pentru prima dată din cenușă datorită publicării unei dizertații în revista ZhRFM a Societății Ruse de Fizică. După moartea subită a lui D.I Mendeleev și decesul fidelilor săi colegi științifici din Societatea Fizico-Chimică Rusă, fiul prietenului și colegului lui D.I Mendeleev în cadrul Societății, Boris Nikolaevich Menshutkin, a ridicat mai întâi mâna către creația nemuritoare a lui Mendeleev. Desigur, Menshutkin nu a acționat singur - el a executat doar ordinul. La urma urmei, noua paradigmă a relativismului a necesitat abandonarea ideii de eter mondial; și de aceea această cerință a fost ridicată la rangul de dogmă, iar opera lui D.I Mendeleev a fost falsificată. Principala distorsiune a Tabelului este transferul „grupului zero” al Tabelului la capătul său, la dreapta, și introducerea așa-numitului. „perioade”. Subliniem că o astfel de manipulare (doar la prima vedere, inofensivă) este explicabilă logic doar ca o eliminare conștientă a verigii metodologice principale din descoperirea lui Mendeleev: sistemul periodic de elemente la începutul său, sursa, adică. în colțul din stânga sus al tabelului, trebuie să aibă un grup zero și un rând zero, unde se află elementul „X” (conform lui Mendeleev - „Newtoniu”), - i.e. difuzare mondială. Pentru a confirma cele de mai sus, îi dăm cuvântul însuși D.I Mendeleev. „... Dacă analogii argonului nu dau deloc compuși, atunci este evident că este imposibil să se includă oricare dintre grupurile de elemente cunoscute anterior și pentru ei ar trebui să se deschidă un grup special zero... Această poziție a analogii de argon din grupul zero este o consecință strict logică a înțelegerii legii periodice și, prin urmare (plasarea în grupul VIII este clar incorectă) a fost acceptată nu numai de mine, ci și de Braizner, Piccini și alții... Acum, când a devenit dincolo de nici cea mai mică îndoială că înaintea acelei grupe I, în care trebuie plasat hidrogenul, există un grup zero, ai cărui reprezentanți au greutăți atomice mai mici decât cele ale elementelor din grupa I, mi se pare imposibil de negat existența. de elemente mai ușoare decât hidrogenul.
Dintre acestea, să acordăm mai întâi atenție elementului din primul rând al primului grup. O notăm cu „y”. Va avea, evident, proprietățile fundamentale ale gazelor argon... „Coroniu”, cu o densitate de aproximativ 0,2 față de hidrogen; și nu poate fi în niciun fel eterul lumii. Acest element „y”, totuși, este necesar pentru a ne apropia mental de cel mai important și, prin urmare, cel mai rapid element „x”, care, după înțelegerea mea, poate fi considerat eter. Aș dori să-l numesc provizoriu „Newtoniu” - în onoarea nemuritorului Newton... Problema gravitației și problema oricărei energii (!!! - V. Rodionov) nu poate fi imaginată ca fiind rezolvată cu adevărat fără o înțelegere reală a eterului ca mediu mondial care transmite energie la distanţe. O înțelegere reală a eterului nu poate fi realizată ignorând chimia lui și neconsiderându-l o substanță elementară; substanțele elementare sunt acum de neconceput fără subordonarea lor legii periodice” („An Attempt at a Chemical Understanding of the World Ether.” 1905, p. 27).
„Aceste elemente, în funcție de mărimea greutăților lor atomice, au ocupat un loc precis între halogenuri și metale alcaline, așa cum a arătat Ramsay în 1900. Din aceste elemente este necesar să se formeze un grup zero special, care a fost recunoscut pentru prima dată de Errere în Belgia în 1900. Consider că este util să adaug aici că, judecând direct după incapacitatea de a combina elementele grupului zero, analogii argonului ar trebui plasați înaintea elementelor grupului 1 și, în spiritul sistemului periodic, să ne așteptăm la o greutate atomică mai mică decât pentru metale alcaline. Este exact ceea ce s-a dovedit a fi. Și dacă da, atunci această împrejurare, pe de o parte, servește ca confirmare a corectitudinii principiilor periodice și, pe de altă parte, arată în mod clar relația dintre analogii argonului și alte elemente cunoscute anterior. Ca urmare, este posibil să se aplice principiile analizate chiar mai pe scară largă decât înainte și să se aștepte elemente din seria zero cu greutăți atomice mult mai mici decât cele ale hidrogenului. Astfel, se poate arăta că în primul rând, mai întâi înaintea hidrogenului, există un element al grupului zero cu greutatea atomică de 0,4 (poate că acesta este coronium lui Yong), iar în rândul zero, în grupul zero, există este un element limitator cu o greutate atomică neglijabil de mică, incapabil de interacțiuni chimice și, ca urmare, posedă o mișcare parțială (gaz) proprie extrem de rapidă. Aceste proprietăți, probabil, ar trebui atribuite atomilor eterului mondial omniprezent (!!! - V. Rodionov). Am indicat această idee în prefața acestei publicații și într-un articol de jurnal rusesc din 1902...” („Fundamentals of Chemistry.” Ed. VIII, 1906, p. 613 și urm.) Din comentarii: Pentru chimie, tabelul periodic modern al elementelor este suficient. Rolul eterului poate fi util în reacțiile nucleare, dar acest lucru nu este foarte semnificativ. Cea mai simplă dovadă a prezenței eterului: Fenomenul de anihilare a unei perechi pozitron-electron și apariția acestei perechi din vid, precum și imposibilitatea prinderii unui electron în repaus. De asemenea, câmpul electromagnetic și o analogie completă între fotonii în vid și undele sonore - fononi în cristale. Eterul este materie diferențiată, ca să spunem așa, atomi în stare dezasamblată, sau mai corect, particule elementare din care se formează viitorii atomi. Prin urmare, nu are loc în tabelul periodic, deoarece logica construirii acestui sistem nu implică includerea structurilor neintegrale, care sunt atomii înșiși. În caz contrar, este posibil să găsiți un loc pentru quarci, undeva în prima perioadă minus. Chimia este un subiect fascinant, dar dificil. Și dacă școala nu avea încă rechizite pentru efectuarea experimentelor, atunci putem spune că a trecut complet. Dar există ceva pe care fiecare persoană ar trebui să înțeleagă cel puțin minim. Acesta este tabelul periodic. Pentru școlari, a învăța este o adevărată tortură. Dacă o văd în vise, atunci numai cele de coșmar. Sunt atât de multe elemente, fiecare cu propriul său număr... Dar o mamă a multor copii a venit cu un mod distractiv cum să înveți tabelul periodic. Este potrivit atât pentru copii, cât și pentru adulți, iar reacția vă va spune cu bucurie despre asta „Atât de simplu!”.
Tabelul periodic al elementelor chimiceDupă cum arată mama a patru copii, Karin Tripp, cu abordarea corectă, este posibil să înveți orice. Să se alăture studiind chimia chiar și copiii mici, ea a decis să transforme tabelul periodic al elementelor într-un câmp de luptă pentru bătălii navale.
Jocul conține patru pagini cu tabelul periodic - două pentru fiecare jucător. Fiecare jucător trebuie să-și deseneze navele pe o masă și, pe cealaltă, să marcheze loviturile și navele avariate ale inamicului cu puncte.
Regulile luptei navale sunt aceleași ca în jocul clasic. Doar pentru a doborî barca unui adversar, trebuie să numiți nu o literă cu un număr, ci elementul chimic corespunzător.
Această tehnică va permite copiilor nu numai să învețe numele elementelor chimice. Promovează dezvoltarea memoriei și a gândirii logice. La urma urmei, copiii vor analiza numerele de serie și culorile.
Pentru ca copiii să găsească mai ușor elementul potrivit la început, rândurile și coloanele ar trebui numerotate. Dar, potrivit lui Karin, copiii ei, după doar câteva zile în care au jucat „bătălia chimică pe mare”, au început să înțeleagă perfect tabelul periodic. Ei cunoșteau chiar și masele atomice și numerele de serie ale elementelor.
În timp, regulile jocului se pot complica. De exemplu, plasarea unei nave numai într-o familie de elemente chimice.
Chiar și fiica de opt ani a unei mame inventive care nu a studiat încă chimia la școală se bucură de acest joc. Și pentru adulți, aceasta este o modalitate grozavă de a se distra.
Toate paginile tabelului periodic pentru jocul bătăliei pe mare pot fi tipărite pe o imprimantă obișnuită sau color și utilizate de un număr nelimitat de ori.
|
| Citire: |
|---|
Popular:
Nou
- Unde au loc cel mai des cutremure?
- Engleza de la zero: cum să începeți să învățați cu succes
- Copiii se gătesc singuri: rețete simple ilustrate
- Ce poți găti pentru un copil de 2 ani?
- Analiza gramaticală a propozițiilor în limba rusă: exemple
- Care sunt simptomele și tratamentul orhitei cauzele orhitei
- Căderea lui Tobruk Secțiunile acestei pagini
- Diabetul insipid, ce este?
- Horoscopul Capricornului pietre talismane după data nașterii
- Semnificația numelui Murad și soarta lui









 Un alt tabel util este seria de activități metalice. Toate metalele sunt situate în el în funcție de grade crescânde de potențial electrochimic. Seria tensiunilor metalice începe cu litiu și se termină cu aur. Se crede că, cu cât mai la stânga un metal ocupă un loc într-un rând dat, cu atât este mai activ în reacțiile chimice. Astfel, cel mai activ metal Litiul este considerat un metal alcalin. Lista de elemente conține și hidrogen spre final. Se crede că metalele situate după el sunt practic inactive. Acestea includ elemente precum cuprul, mercurul, argintul, platina și aurul.
Un alt tabel util este seria de activități metalice. Toate metalele sunt situate în el în funcție de grade crescânde de potențial electrochimic. Seria tensiunilor metalice începe cu litiu și se termină cu aur. Se crede că, cu cât mai la stânga un metal ocupă un loc într-un rând dat, cu atât este mai activ în reacțiile chimice. Astfel, cel mai activ metal Litiul este considerat un metal alcalin. Lista de elemente conține și hidrogen spre final. Se crede că metalele situate după el sunt practic inactive. Acestea includ elemente precum cuprul, mercurul, argintul, platina și aurul.