Bagian situs
Pilihan Editor:
- Cara membuat lokomotif uap dan transportasi darat lainnya melakukannya sendiri
- Mangkok minum itik untuk Anda sendiri: fitur pembuatan
- Tata ruang apartemen dalam serangkaian kubus 2
- Lakukan sendiri dari hal-hal yang tidak perlu: pekarangan, kebun, kebun dapur
- Konstruksi kapal motor aluminium yang dilas "ajaib" Konstruksi kapal aluminium
- Pom bensin rumah
- Drywall Carrier: Sederhana dan Nyaman
- Grousers: attachment untuk traktor berjalan di belakang
- Bahan untuk perbaikan sendiri bumper plastik. Memperbaiki bumper plastik
- Membuat tabel milling dengan tangan Anda sendiri: gambar, video dan foto
Iklan
| Berapa laju perambatan nyala normal. Api menyebar di atas permukaan cair |
|
3. DISTRIBUSI Api PADA CAMPURAN GAS Kecepatan perambatan nyala api selama pembakaran zat padat, cair dan gas adalah kepentingan praktis dalam hal mencegah kebakaran dan ledakan. Pertimbangkan kecepatan perambatan nyala api dalam campuran gas dan uap yang mudah terbakar dengan udara. Mengetahui kecepatan ini, dimungkinkan untuk menentukan laju aliran udara-gas yang aman di pipa, poros, instalasi ventilasi, dan sistem bahan peledak lainnya. 3.1. KECEPATAN DISTRIBUSI FLAME Sebagai contoh dalam gambar. 3.1 adalah diagram ventilasi gas buang di tambang batubara. Dari drift tambang 1 hingga pipa 2, campuran debu udara dan batu bara yang berdebu dihilangkan, dan dalam beberapa kasus, metana dilepaskan dalam lapisan batu bara. Jika sumber penyalaan terjadi, nyala depan 3 akan merambat ke arah drift 1. Jika kecepatan campuran yang mudah terbakar w akan kurang dari kecepatan rambat depan api dan relatif terhadap dinding tabung, nyala api akan menyebar ke poros dan menyebabkan ledakan. Oleh karena itu, untuk pengoperasian normal sistem ventilasi, kondisinya harus dipenuhi w\u003e kamu. Tingkat penghilangan campuran bahan peledak harus lebih besar dari kecepatan rambat permukaan api. Ini akan mencegah masuknya nyala api ke drift tambang. Fig. 3.1. Pola distribusi api di tambang: 1 - milikku; 2 - pipa; 3 - depan api Teori propagasi nyala, dikembangkan dalam karya Ya.B. Zeldovich dan D.A. Frank-Kamenetsky, berdasarkan persamaan konduksi panas, difusi, dan kinetika kimia. Pengapian campuran yang mudah terbakar selalu dimulai pada satu titik dan menyebar ke seluruh volume yang ditempati oleh campuran yang mudah terbakar. Pertimbangkan wadah satu dimensi - tabung diisi dengan campuran yang mudah terbakar (Gbr. 3.2). Jika campuran dinyalakan dari salah satu ujung tabung, bagian depan nyala api yang sempit akan merambat di sepanjang tabung, memisahkan produk pembakaran (di belakang bagian depan nyala) dari campuran yang mudah terbakar segar. Bagian depan nyala berbentuk topi atau kerucut, bagian cembung menghadap pergerakan nyala. Bagian depan nyala api adalah lapisan gas tipis dengan lebar (10 -4 ÷ 10 -6) m. Pada lapisan ini, yang disebut zona pembakaran, reaksi pembakaran kimia terjadi. Temperatur bagian depan nyala, tergantung pada komposisi campuran, adalah T \u003d (1500 ÷ 3000) K. Panas pembakaran yang dibebaskan dihabiskan untuk memanaskan produk pembakaran dari campuran yang mudah terbakar baru dan dinding tabung karena proses konduksi panas dan radiasi.
Fig. 3.2. Pola rambat depan api dalam sebuah tabung Ketika nyala depan bergerak dalam tabung dalam campuran yang mudah terbakar, gelombang kompresi muncul yang menciptakan gerakan pusaran. Vortisitas gas menekuk api bagian depan, tanpa mengubah ketebalannya dan sifat proses yang terjadi di dalamnya. Pada unit permukaan depan api, jumlah materi yang sama per satuan waktu selalu menyala Setiap elemen depan api dS bergerak relatif terhadap campuran segar selalu dalam arah normal ke depan api pada titik tertentu (Gbr. 3.2), dan kecepatan gerakan ini: di mana kepadatan campuran mudah terbakar segar. Nilai disebut kecepatan rambat api normal dan memiliki dimensi m / s. Ini adalah nilai konstan dari proses pembakaran campuran ini dan tidak tergantung pada kondisi hidrodinamik yang menyertai proses pembakaran. Kecepatan nyala normal selalu lebih kecil dari kecepatan yang diamati. dan, yaitu, kecepatan depan pembakaran relatif terhadap dinding tabung: kamu< u . Jika bagian depan nyala rata dan terarah tegak lurus terhadap sumbu tabung, maka dalam hal ini kecepatan rambat nyala yang diamati dan normal akan sama. u n \u003d kamu. Area depan nyala cembungS vyp selalu lebih dari area depan yang datar S PLoleh karena itu > 1. Kecepatan rambat nyala normalkamu untuk setiap campuran yang mudah terbakar tergantung pada ketidakmurnian gas inert, suhu campuran, kelembaban dan faktor lainnya. Secara khusus, pemanasan awal gas yang mudah terbakar meningkatkan kecepatan perambatan nyala api. Dapat ditunjukkan bahwa kecepatan rambat nyala api kamusebanding dengan kuadrat dari suhu absolut campuran: u n. \u003d const · T 2. Dalam gbr. Gambar 3.3 menunjukkan ketergantungan kecepatan rambat nyala api dalam campuran "udara - karbon monoksida" yang mudah terbakar tergantung pada konsentrasi CO. Sebagai berikut dari grafik di atas, kecepatan rambat nyala meningkat dengan meningkatnya suhu campuran. Untuk setiap nilai suhu, kecepatan rambat nyala api memiliki maksimum di wilayah konsentrasi karbon monoksida CO ~ 40%. Kecepatan rambat nyala dipengaruhi oleh kapasitas panas dari gas inert. Semakin besar kapasitas panas dari gas inert, semakin banyak menurunkan suhu pembakaran dan semakin banyak mengurangi kecepatan perambatan api. Jadi, jika campuran metana dengan udara diencerkan dengan karbon dioksida, maka kecepatan rambat nyala bisa berkurang 2-3 kali. Laju perambatan nyala dalam campuran karbon monoksida dengan udara sangat dipengaruhi oleh kelembaban yang terkandung dalam campuran, keberadaan partikel jelaga dan ketidakmurnian gas inert.
Fig. 3.3. Tingkat propagasi api dari konsentrasi karbon monoksida dalam campuran Tingkat pembakaran laminar - kecepatan di mana api depan bergerak ke arah tegak lurus ke permukaan rakitan bahan bakar segar.
Pembakaran bergolak.
Kecepatan nyala yang bergejolak - kecepatan gerak depan api dalam aliran turbulen.
Pembakaran laminar tidak menghasilkan laju panas yang diperlukan dalam mesin, oleh karena itu turbulensi aliran gas diperlukan. Persamaan Arrhenius:
Pengaruh berbagai faktor pada proses pembakaran di mesin pembakaran internal dengan percikan api.Komposisi campuran.
Rasio kompresi.
 Dengan peningkatan kecepatan, fase pengapian meningkat, yang mengarah pada keterlambatan pengembangan proses pembakaran dan penurunan jumlah panas yang dilepaskan per siklus. Karena itu, ketika berubah Waktu pengapian Waktu pengapian - sudut rotasi poros engkol dari saat mengajukan percikan ke TDC.
P
Pelanggaran utama dari proses pembakaran di mesin pembakaran internal dengan percikan api. Peledakan.D
Dengan ledakan: Bercermin dari dinding ruang bakar, gelombang kejut membentuk bagian depan api sekunder dan pusat penyalaan sendiri. Secara lahiriah, ledakan dimanifestasikan dalam bentuk ketukan tuli ketika mesin beroperasi pada beban tinggi. Konsekuensi dari operasi mesin dengan ledakan: Overheating dan pembakaran komponen mesin individual (katup, piston, paking kepala, elektroda busi); Kerusakan mekanis pada bagian-bagian mesin karena beban kejut; Penurunan kekuatan dan profitabilitas pekerjaan. T.O. kerja panjang dengan peledakan tidak bisa diterima. P  Kemampuan bahan bakar untuk penyalaan sendiri menjadi ciri khas ketukan resistensi dan resistensi ketukan diperkirakan angka oktan (OCH) . Och - secara numerik sama dengan fraksi volume isooctane yang berdononasi buruk dari campuran dengan heptana normal yang mudah ditonasikan, setara dengan bensin dalam sifat peledakan. Isooctane - 100 unit, heptane normal - 0 unit. Sebagai contoh: angka oktan 92 berarti bahwa bensin ini memiliki ketahanan peledakan yang sama dengan campuran referensi 92% isooctane dan 8% heptana normal. A dan - metode penelitian untuk memproduksi bensin; metode m - motor (huruf biasanya tidak ditulis). Dalam metode uji motorik, tingkat kompresi dikontrol hingga detonasi dimulai, dan angka oktan ditentukan dari tabel. Metode motorik mensimulasikan mengemudi dengan muatan penuh (truk keluar kota). Metode penelitian meniru gerakan pada beban parsial (di kota).
Jika angka oktan terlalu besar, maka kecepatan rambat nyala berkurang. Proses pembakaran tertunda, yang mengarah pada penurunan efisiensi dan peningkatan suhu gas buang. Konsekuensi dari ini adalah penurunan daya, peningkatan konsumsi bahan bakar, overheating mesin dan pembakaran elemen individu. Performa mesin maksimum dicapai dengan jumlah oktan bahan bakar yang dekat dengan ambang detonasi. Cara menangani peledakan: 
TerbakarIni adalah reaksi oksidatif kimia yang intens yang disertai dengan panas dan luminositas. Pembakaran terjadi ketika ada bahan yang mudah terbakar, zat pengoksidasi, dan sumber penyulutan. Oksigen, asam nitrat dapat bertindak sebagai agen pengoksidasi dalam proses pembakaran. Sebagai bahan bakar - banyak senyawa organik, belerang, hidrogen sulfida, pirit, sebagian besar logam dalam bentuk bebas, karbon monoksida, hidrogen, dll. Dalam api sungguhan, zat pengoksidasi selama pembakaran biasanya adalah oksigen atmosfer. Manifestasi eksternal dari pembakaran adalah nyala api, yang ditandai dengan cahaya dan panas. Ketika sistem pembakaran hanya terdiri dari fase padat atau cair atau campurannya, nyala mungkin tidak terjadi, mis., Terjadi tanpa cacat terbakar atau membara. Tergantung pada keadaan agregasi bahan awal dan produk pembakaran, pembakaran homogen, pembakaran bahan peledak, pembakaran heterogen dibedakan. Pembakaran homogen. Dengan pembakaran homogen, bahan awal dan produk pembakaran berada dalam kondisi agregasi yang sama. Jenis ini termasuk pembakaran campuran gas (gas alam, hidrogen, dll. Dengan zat pengoksidasi, biasanya oksigen udara) / Pembakaran eksplosif karena transisi suatu zat dari keadaan terkondensasi ke gas. Pembakaran heterogen. Dalam pembakaran heterogen, bahan awal (misalnya, bahan bakar padat atau cair dan zat pengoksidasi gas) berada dalam keadaan agregat yang berbeda. Proses teknologi paling penting dari pembakaran heterogen adalah pembakaran batu bara, logam, pembakaran bahan bakar cair dalam tungku minyak, mesin pembakaran internal, dan ruang bakar mesin roket. Pergerakan nyala melalui campuran gas disebut penyebaran api. Bergantung pada kecepatan rambat api pembakaran, dapat berupa deflagrasi dengan kecepatan beberapa m / s, ledakan - kecepatan urutan puluhan dan ratusan m / s dan ledakan - dari seribu m / s. Pembakaran deflagrasi dibagi menjadi laminar dan turbulen. Pembakaran laminar ditandai dengan laju perambatan nyala yang normal. Kecepatan rambat api normal, disebut kecepatan depan api relatif terhadap gas yang tidak terbakar, dalam arah yang tegak lurus terhadap permukaannya. Suhu yang relatif sedikit meningkatkan kecepatan normal perambatan nyala, pengotor inert menguranginya, dan peningkatan tekanan mengarah pada peningkatan atau penurunan kecepatan. Dalam aliran gas laminar, kecepatan gasnya kecil. Laju pembakaran dalam hal ini tergantung pada laju pembentukan campuran yang mudah terbakar. Dalam nyala yang bergejolak, pusaran gas meningkatkan pencampuran gas yang bereaksi, karena permukaan melalui mana peningkatan difusi molekuler. Indikator bahaya kebakaran dan ledakan gas. Karakteristik dan ruang lingkup merekaBahaya kebakaran proses teknologi sebagian besar ditentukan oleh sifat fisikokimia bahan baku, produk antara dan akhir yang beredar dalam produksi. Indikator bahaya kebakaran dan ledakan digunakan dalam kategorisasi kamar dan bangunan, dalam pengembangan sistem untuk memastikan keselamatan kebakaran dan keselamatan ledakan. Gas adalah zat yang tekanan uap absolutnya pada suhu 50 ° C sama dengan atau lebih dari 300 kPa atau yang suhu kritisnya kurang dari 50 ° C. Untuk gas, indikator berikut berlaku: Kelompok mudah terbakar-indikator yang berlaku untuk semua negara agregat. Mudah terbakar - kemampuan suatu bahan atau bahan untuk terbakar. Mudah terbakar bahan dan bahan dibagi menjadi tiga kelompok. Tidak mudah terbakar (tidak mudah terbakar) - zat dan bahan yang tidak dapat terbakar di udara. Zat yang tidak mudah terbakar dapat terbakar (misalnya, zat pengoksidasi, serta zat yang mengeluarkan produk yang mudah terbakar ketika berinteraksi dengan air, oksigen, atau satu sama lain). Tidak mudah terbakar (sulit terbakar) - zat dan bahan yang dapat menyala di udara dari sumber penyulut, tetapi tidak dapat terbakar secara independen setelah dilepaskan. Mudah terbakar (Mudah terbakar) - zat dan bahan yang dapat menyala secara spontan, serta terbakar dari sumber penyulut dan terbakar secara independen setelah dilepaskan. Zat dan bahan yang mudah terbakar dibedakan dari kelompok bahan dan bahan yang mudah terbakar. Mudah terbakar disebut bahan dan bahan mudah terbakar yang dapat menyala dari paparan jangka pendek (hingga 30 detik) ke sumber penyulut berenergi rendah (cocokkan api, percikan, rokok yang membara, dll.). Mudah terbakar gas ditentukan secara tidak langsung: gas yang memiliki batas konsentrasi pengapian di udara disebut bahan bakar; jika gas tidak memiliki batas konsentrasi penyalaan, tetapi nyala sendiri pada suhu tertentu, itu disebut tahan api; dengan tidak adanya batas pengapian konsentrasi dan suhu penyalaan otomatis, gas disebut tidak mudah terbakar. Dalam praktiknya, kelompok yang mudah terbakar digunakan untuk membagi bahan yang mudah terbakar, ketika menetapkan kelas zona peledak dan bahaya kebakaran menurut EMP, ketika menentukan kategori bangunan dan bangunan untuk ledakan dan bahaya kebakaran, ketika mengembangkan langkah-langkah untuk memastikan keselamatan kebakaran dan ledakan peralatan dan bangunan. Suhu penyalaan otomatis - suhu terendah zat, di mana, di bawah kondisi pengujian khusus, ada peningkatan tajam dalam laju reaksi eksotermik yang berakhir dengan pembakaran nyala api. Batas konsentrasi perambatan api (pengapian) - itu rentang konsentrasi di mana pembakaran campuran uap dan gas yang mudah terbakar dengan udara atau oksigen dimungkinkan. Batas konsentrasi perambatan nyala api yang lebih rendah (atas) adalah minimum (maksimum) kandungan bahan bakar dalam campuran adalah media pengoksidasi bahan yang mudah terbakar ”di mana nyala dapat merambat melalui campuran pada jarak berapa pun dari sumber nyala. Di dalam batas-batas ini, campuran itu mudah terbakar, dan di luarnya, campuran itu tidak mampu terbakar. Batas suhu perambatan nyala (pengapian) adalah suhu suatu zat di mana uap jenuhnya membentuk konsentrasi dalam media pengoksidasi tertentu yang sama dengan batas konsentrasi perambatan api yang lebih rendah (batas suhu bawah) dan batas atas (batas suhu atas). Kemampuan untuk meledak dan terbakar ketika berinteraksi dengan air, oksigen atmosfer dan zat lainnya - Indikator kualitas yang mencirikan bahaya kebakaran tertentu dari zat tertentu. Properti zat ini digunakan dalam menentukan kategori produksi, serta dalam memilih kondisi yang aman untuk melakukan proses teknologi dan kondisi untuk penyimpanan bersama dan pengangkutan bahan dan bahan. |
PelumasTujuan utama dalam pengembangan pelumas yang ramah lingkungan adalah menciptakan produk dengan biodegradabilitas tinggi dan ekotoksisitas rendah. Di negara - negara maju di Barat perusahaan-perusahaan negara dan swasta sekarang mulai menciptakan pasar pelumas yang ramah lingkungan. Sebagian besar penelitian berfokus pada komposisi kimia produk dan penilaian biodegradabilitasnya. Saat membuat pelumas yang ramah lingkungan, dua bidang utama dipertimbangkan: produksi minyak dasar, sifat kimianya menentukan sifat dampak pada lingkungan, dan sintesis aditif baru - ramah lingkungan, ramah lingkungan, dan efektif. Saat ini, dan mungkin untuk masa depan, tiga kelompok minyak dasar yang diperoleh dari berbagai bahan baku sangat penting: minyak hidro-retak (HA), polyalphaolefins (PAO) dan ester yang mengalami biodegradasi cepat di lingkungan. Minyak dasar dari sistem aliran tradisional tidak diragukan lagi akan tetap sangat penting untuk jangka waktu yang tidak terbatas, terutama dengan mempertimbangkan fakta bahwa pelumas diperoleh berdasarkan PAO. ester polialkohol, glikol polialkilena dan diester, memiliki biaya 2-10 kali lebih banyak daripada produk minyak bumi. Peningkatan biodegradabilitas bukanlah insentif untuk mengatasi perbedaan harga. Performa tinggi dan ramah lingkungan dari minyak mineral disediakan oleh serangkaian kualitas tertentu. Pertama-tama, itu adalah komposisi kimia kelompok fraksinya yang sempit dan menguntungkan dengan jumlah minimum senyawa sulfur dan nitrogen dalam minyak dasar. Pemilihan bahan baku, pemilahan minyak yang digunakan dalam produksi minyak indeks tinggi, dan pemrosesan terpisahnya adalah sangat penting. Dalam persiapan minyak mineral dasar yang memenuhi persyaratan lingkungan, pemurnian selektif memainkan peran penting. membakar karsinogenisitas produk. Saat ini, di AS dan Kanada, lebih dari 70% minyak dasar diperoleh dengan pemurnian selektif. Penerapan proses modern seperti hydrocracking, hydrodewaxing, hydroisomerization membuka peluang besar. Teknologi ini dijelaskan secara rinci dalam pekerjaan. Penggunaan proses hidrokatalitik dalam kombinasi dengan metode tradisional pemurnian bahan baku minyak dengan pelarut selektif meningkatkan sifat operasional dan lingkungan dari minyak dasar. Di atas meja. 1.4 menunjukkan data komparatif pada komposisi kimia dari minyak dasar yang diperoleh dengan menggunakan perawatan selektif dan perawatan hydrot. Yang terakhir ini secara signifikan mengurangi kandungan arena, sulfur dan nitrogen dalam minyak. Tabel 14 Efek hydrotreating pada komposisi kimia minyak dasar Pengenalan proses hydrocracking dan hidroisomerisasi dalam produksi minyak mineral dasar memungkinkan untuk memperoleh produk-produk dari peningkatan biodegradabilitas dan tidak mengandung aren. Minyak hydrocracking, menurut hasil yang diperoleh dengan menggunakan metode tes modern, tidak beracun, tidak adanya arena di dalamnya menunjukkan karsinogenisitas yang sangat rendah dan kemungkinan pertumbuhannya tidak signifikan melalui pembentukan dan akumulasi arena poliklik selama operasi; kurangnya arena dan dominasi pemberian isoparaffin memberikan biodegradabilitas yang cukup tinggi. Di AS, minyak hydrocracking dasar telah diproduksi sejak akhir tahun 1996. . Disiapkan untuk meluncurkan instalasi di Finlandia. Di Rusia, VNIINP, bersama dengan pusat sains dan teknik OAO LUKOIL dan JSC LUKOIL-Volgogradneftepererabotka, melakukan penelitian pada organisasi produksi sejumlah minyak dan pangkalan yang langka menggunakan teknologi hidrogenasi, khususnya, minyak penerbangan MS-8 dan fluida hidrolik penerbangan. -10. Dibandingkan dengan minyak mineral, sintetis dalam beberapa kasus memiliki karakteristik lingkungan yang lebih baik. Kelas yang paling penting dari minyak sintetis dari sudut pandang keamanan lingkungan termasuk minyak yang dibuat berdasarkan ester sintetis, polyalphaolefin dan polibuten. Mereka tidak beracun, non-karsinogenik, ditandai dengan rendahnya emisi zat berbahaya. Oli sintetik berbasis ester dengan aditif dari tahun 60-an banyak digunakan dalam mesin turbin gas pesawat sipil dan militer. Di TsIAM, bersama-sama dengan VNIINP dan 25 Lembaga Penelitian Negara dari Kementerian Pertahanan Federasi Rusia, pekerjaan sedang dilakukan untuk membuat minyak ester bilyyugo (hingga 240 ° C) dengan suhu tinggi menggunakan komposisi aditif efektif yang tidak kalah kualitasnya dengan minyak asing terbaik. Analisis informasi ilmiah, teknis dan paten tentang minyak untuk mesin turbin gas penerbangan menunjukkan bahwa poliol ester tetap menjadi kelas utama senyawa untuk digunakan sebagai basa dasar [PO]. Namun, situasinya berubah dengan mesin pesawat generasi berikutnya, karena perbaikan desain dan kebutuhan untuk mengurangi konsumsi bahan bakar menyebabkan peningkatan tekanan, suhu dan beban oli. Yang terakhir berkontribusi pada risiko simpanan karbon lokal. Oleh karena itu, untuk penerbangan militer di masa depan, perlu untuk meninggalkan penggunaan minyak berbasis ester. Untuk tujuan ini, minyak yang paling menjanjikan dari jenis baru adalah yang didasarkan pada perfluoroalkylpolyethers sederhana. Menurut data modern, senyawa ini tidak beracun dan bahkan digunakan di luar negeri dalam parfum dan untuk konservasi monumen marmer seni dan arsitektur. Aditif memiliki pengaruh besar pada sifat lingkungan pelumas. Dalam minyak penerbangan, antioksidan tradisional dan inhibitor korosi seperti dioctyl diphenylamine, phenyl - naphthylamine, benzotriazole, aditif K-51 dari jenis suksinimida dan lainnya yang telah terbukti sendiri banyak digunakan sebagai aditif. Di seluruh dunia, pekerjaan telah berlangsung lama untuk menciptakan produk baru yang tidak beracun dan dapat terurai secara hayati. Secara khusus, sejak tahun 90-an, pengembangan pengganti aditif klorin telah dilakukan. Masalah penting adalah penggantian senyawa timbal. Pengganti timbal adalah senyawa bismut. Pengembangan aditif bismuth dithiocarbamate telah dimulai. Aditif seperti Mif-1 (aditif dengan komposisi kompleks dari jenis benzena), Irganox L-57 (aditif antioksidan dari Siba, diphenylamine botol dan diphenylamine dalam kemasan), aditif "X" (senyawa yang mengandung fluor dengan gugus fungsi oksisulfit dan hidroksikarbat) dikembangkan. Sifat-sifat aditif yang dikenal ditingkatkan. Dengan demikian, kandungan isomer ureo neutrotoxic dalam tricresylphosphate berkurang menjadi 3% (Rusia), dan tricresylphosphate yang tidak mengandung ortoomer diproduksi di AS. Bahaya kebakaran dan ledakan bahan bakar dan pelumas Bahan bakar dan pelumas yang saat ini digunakan adalah produk-produk berbahaya. Dalam baku tembak, bahan bakar gas sangat berbahaya. Bahan bakar hidrokarbon (bahan bakar jet, gasolin, dll.) Adalah cairan yang mudah terbakar (LVF). Mereka dicirikan oleh ketahanan api yang tinggi (-2000 ° С) dan volatilitas, mereka dengan mudah membuat campuran yang mudah terbakar dengan udara, yang, ketika dibakar, membentuk sejumlah besar produk pembakaran (koefisien stoikiometrik besar), yang merupakan dielektrik yang baik dan, oleh karena itu, dapat mengakumulasi muatan listrik statis. Menurut bahaya kebakaran, cairan yang mudah terbakar dibagi menjadi tiga kategori. Titik nyala digunakan sebagai indikator penentu (ditentukan berdasarkan GOST 12.1.044-89): Bergantung pada suhu penyalaan otomatis (ditentukan berdasarkan GOST 12.1.044-89), bahan bakar hidrokarbon termasuk dalam satu atau beberapa kelompok campuran peledak uap dengan udara: Kami mengukur uap bahan bakar hidrokarbon dengan udara yang termasuk dalam kategori bahaya ledakan TTA: ditentukan berdasarkan GOST 12.1.011-78. Indikator ini digunakan ketika memilih jenis peralatan listrik tahan ledakan dan dalam desain alat pemadam kebakaran. Sifat berbahaya api bahan bakar juga ditentukan oleh batas konsentrasi penyalaan (CPV) - kandungan minimum dan maksimum uap bahan bakar dalam campuran dengan udara (zat pengoksidasi), di mana nyala dapat merambat melalui campuran pada jarak berapa pun dari sumber pengapian (GOST 12.1.044-89). Karakteristik penting bahan bakar adalah batas suhu penyalaan, suhu di mana uap bahan bakar jenuh di udara masing-masing dalam konsentrasi sama dengan CPV bawah atau atas. Energi pelepasan listrik minimum yang diperlukan untuk menyalakan campuran uap-udara itu penting. Ketika menilai bahaya kebakaran selama penanganan bahan bakar, laju pembakaran juga ditentukan - jumlah bahan bakar yang dibakar per unit waktu dari permukaan unit; energi penyalaan minimum - untuk memastikan keamanan intrinsik elektrostatik. Interaksi pembakaran bahan bakar dengan bahan pemadam berbasis air dinilai (menurut GOST 12.1.044-89). Api sering didahului oleh ledakan campuran udara-gas. Dengan ledakan campuran udara dalam pipa berdiameter besar dan panjang, pembakaran detonasi dapat terjadi, merambat pada kecepatan 1100-1400 m / s. Tekanan dapat meningkat menjadi 0,8 MPa atau lebih. Gelombang kejut berkecepatan tinggi menyebabkan peningkatan tajam dalam tekanan, suhu dan kepadatan campuran yang mudah terbakar, yang, pada gilirannya, mempercepat reaksi kimia pembakaran dan meningkatkan efek destruktif. Konsentrasi uap bahan bakar yang eksplosif dengan udara dapat terbentuk dalam kisaran suhu yang luas dan terutama di ruang dan wadah tertutup. Sifat dan isi dari tindakan pencegahan diatur oleh instruksi departemen khusus. Inti dari tindakan pencegahan adalah untuk mencegah terjadinya sumber pemanasan, terutama nyala api terbuka, di tempat-tempat di mana campuran eksplosif terbentuk. Salah satu sumber api terbuka yang paling berbahaya adalah pembuangan potensi elektrostatik melalui media udara-uap dan pembentukan percikan selama dampak padatan. Terjadinya potensi listrik yang tinggi pada bahan bakar dijelaskan oleh sifat elektrofisika. Mereka dapat dicirikan oleh kemampuan untuk mengakumulasi biaya dalam volume (kemampuan elektrolisis) dan biaya sifat relaksasi (kabel listrik). Di atas meja. 1.5. Indikator yang mencirikan sifat bahaya kebakaran dari bahan bakar penerbangan diberikan. Tabel 1.5 Sifat bahaya kebakaran dari bahan bakar penerbangan 1 Dihitung berdasarkan aditivitas. ^ Dihitung menurut persamaan (47) dan (48) GOST 12.1.044-89 pada titik didih -10 / -4 ° С. Dalam pembilang - dalam wadah tertutup, dalam penyebut - di tempat terbuka. a limits Batas perambatan api menurut GOST 10277-89. Kecepatan rambat nyala normalKecepatan rambat nyala api dalam campuran yang mudah terbakar tergantung pada kondisi penentuan dan rujukannya. Untuk penilaian komparatif bahan bakar dari karakteristik ini, kecepatan rambat api normal diadopsi - ini adalah kecepatan linier dari zona pembakaran sehubungan dengan campuran mudah terbakar homogen segar dalam arah normal ke depan api. Kecepatan rambat nyala dalam kondisi seperti itu untuk komposisi tertentu dari campuran yang mudah terbakar dapat dianggap sebagai karakteristik fisikokimia yang hanya bergantung pada tekanan dan suhu. Secara eksperimental, laju perambatan api normal ditentukan menurut GOST 12.1.044-89. Pada suhu 20 ° C dan tekanan 0,101 MPa dalam campuran karbohidrat-udara-udara, kecepatan maksimum u dicapai ketika konsentrasi bahan bakar dalam campuran adalah C ^ ~ 1,15 C ste x (Gbr. 1.24), mis. pada a - 0,87 dan untuk jumlah atom karbon dalam hidrokarbon n\u003e 7, adalah -39-40 cm / s (Gbr. 1.25). Kecepatan perambatan nyala normal minimum dan laju pembakaran massa yang dicapai pada batas konsentrasi perambatan nyala dalam kondisi normal masing-masing adalah 4-6 cm / s dan (5-7) 10 ° g / (cm 2 s). Dengan tidak adanya data eksperimental, kecepatan rambat nyala api normal harus dipilih dengan interpolasi dari nilai-nilai dan untuk campuran yang serupa dalam sifat fisikokimia, atau persamaan empiris harus digunakan. Persamaan sederhana dan nyaman diusulkan oleh A.S. Pra-mengemudi:
m \u003d m n + B (St-C ^ (C dalam -C t), di mana dan "adalah kecepatan rambat dalam cm / s; t adalah laju pembakaran massa campuran, g / (cm 2 s); dan 11P, t „adalah nilai batas (minimum) dari kecepatan rambat api; С „dan С н - konsentrasi bahan bakar dalam campuran pada batas konsentrasi rendah dan tertinggi dari perambatan api; A dan B adalah koefisien yang ditentukan oleh satu titik eksperimen.  Fig. 1.24. propagasi nyala tergantung pada koefisien stoikiometrik molar udara berlebih Lm:
 Fig. 1.25. Kecepatan rambat nyala api maksimum normal dalam campuran bahan bakar-udara, tergantung pada jumlah atom karbon dalam molekul hidrokarbon (P \u003d 0,101 MPa, 1 \u003d 20 ° C, pipa kaca terbuka: panjang 57 cm, diameter 2,5 cm): - parafin; * - olefinik; ° - asetilena; D - naftenat; di - dnolsfipovye; o siklik (С П П2 „); 1 - bensin [116]; 2 - benzena Hubungan fungsional dari kecepatan rambat api dengan konsentrasi bahan bakar Ct pada Ct C * t (tetapi diberikan oleh EIM) dapat direpresentasikan dengan persamaan:
/ sg s; l "s t-s" t " dimana m dan dan n - Kecepatan rambat nyala api normal pada konsentrasi bahan bakar dalam campuran Ct dan S * t , cm / s; dan hal - sama pada batas konsentrasi yang lebih rendah dari perambatan nyala, cm / s. Kurva Perkiraan dan n - /(Ct) dalam campuran kompleks komposisi dapat dibangun pada tiga titik referensi yang sesuai dengan batas konsentrasi bawah dan atas dan kecepatan rambat nyala api maksimum. Untuk titik-titik ini, konsentrasi bahan bakar dan kecepatan rambat nyala api harus diketahui. Nilai Ct dan dan dan untuk poin tertentu dihitung sesuai dengan prosedur berikut. Setiap campuran kompleks dari gas yang mudah terbakar tampaknya terdiri dari jumlah campuran sederhana yang sesuai. Perhitungan komposisi pada batas konsentrasi dan pada titik kecepatan maksimum dibuat sesuai dengan aturan pencampuran, berdasarkan batas konsentrasi dan komposisi "campuran maksimum". Persamaan perhitungan yang sesuai memiliki bentuk: C] + C * 2 + Soo ....
dimana B - konsentrasi bahan bakar pada CPRP atau dalam campuran dengan laju perambatan api maksimum,% (vol.); C, C 2, C 3, ... adalah konsentrasi gas sederhana dalam campuran kompleks, (s, + C 2 + C 3 + ... \u003d 100%); B |, b 2, b 3\u003e ... adalah konsentrasi gas dalam campuran sederhana pada CPRP atau dalam campuran dengan dan dan,% (vol.). Kecepatan rambat nyala normal maksimum dalam campuran dihitung dengan persamaan; C, g /, + C2i2 + C3y3 + C, + C 2 + c 3 4 -...
di mana C *, C 2, C 3 - isi campuran sederhana dalam campuran kompleks dengan laju perambatan nyala maksimum,% (vol.); dan *, dan 2, dan 3 - kecepatan rambat nyala maksimum dalam campuran sederhana, cm / s. Untuk menghitung titik kurva lainnya dan dan \u003d / (C ;.), Seseorang harus menetapkan beberapa nilai acak dari kecepatan nyala, menemukan konsentrasi b dalam campuran kompleks sesuai dengan persamaan (1.5), di mana C, C 2, C 3 diberikan oleh komposisi campuran. Prosedur perhitungan ini berlaku untuk campuran gas yang memiliki sifat terkait (mis. Metana-propana). Campuran ini tidak berlaku untuk campuran P P N W dengan H3 dan CO. Laju pembakaran massa berbanding lurus dengan suhu absolut dari pemanasan awal campuran dan dapat dihitung dengan persamaan:  dimana w lalu t „R eo - laju pembakaran campuran massa pada suhu T, To dan T P e d , masing-masing, g / (cm-s). Jika T »T pr e D, maka  Ketergantungan dari kecepatan rambat api normal maksimum pada suhu dan tekanan kira-kira dijelaskan oleh persamaan: dan ’ \u003d u1 (T/273) 2 ?(/’/10 5)", (19) di mana i adalah kecepatan rambat api normal maksimum pada suhu 293 K dan tekanan 0,101 MPa, cm / s; T adalah suhu nyala, dalam K; P adalah tekanan pada Pa; p - eksponen, ns tergantung pada tekanan dalam kisaran MO 4 + 5-10 5 Pa; untuk campuran udara-bahan bakar n \u003d -0,3 - *? -0,4; untuk campuran hidrokarbon-oksigen P \u003d -0.1 -5-0. Laju perambatan nyala normal maksimum tergantung pada konsentrasi oksigen dalam zat pengoksidasi PPP Woo P. giil \u003d \\% ig "0 + B- dimana Г „I! Tapi - pada y, n y ^ 0, cm 2 / s; Koefisien B - ditentukan oleh data eksperimen (untuk propana B ~ 0,22); y / t - konsentrasi oksigen yang sangat rendah dalam zat pengoksidasi. Nilai dan * „pada konsentrasi oksigen berbeda dalam zat pengoksidasi 1 // „hlm ketika mengubah suhu pemanasan awal campuran dari 310 menjadi 422 K dapat ditentukan dengan persamaan: ": \u003d Di; (u), (MO di mana dan * „- dalam cm / s; T - dalam K; A, C un - sesuai dengan data eksperimen, nilainya untuk propana, isooctane dan etilen diberikan di bawah ini: Batas konsentrasi dan suhu perambatan nyalaBatas konsentrasi perambatan nyala (CPRP) dalam campuran yang mudah terbakar adalah konsentrasi bahan bakar maksimum dan minimum dalam campuran di mana perambatan nyala masih dimungkinkan (masing-masing batas bawah dan atas). Mereka tergantung pada aktivitas kimia bahan bakar, konsentrasi zat pengoksidasi dan kotoran inert, konduktivitas termal dan kapasitas panas campuran, suhu dan tekanan. CPRP untuk bahan bakar suspensi, berdasarkan pada sifat fisiologis dan kimianya, ditentukan oleh media dispersi. Penentuan KPRP dengan campuran yang mudah terbakar homogen dilakukan sesuai dengan GOST 12.1.044-89: menurut item 4.11 secara eksperimen dan menurut item 4.12 - dengan perhitungan. Menurut GOST 12.1.044-84, batas konsentrasi perambatan nyala api didefinisikan sebagai  di mana С „(i) - CPRP bawah (atas),% (vol.); hal - koefisien stoikiometri (jumlah mol oksigen per mol bahan bakar); tapi dan B - konstanta universal, nilainya diberikan di bawah: Untuk bahan bakar C P N W P \u003d n + t / 4. Kesalahan penghitungan: untuk batas bawah 0,12; untuk 0,40 teratas di (3 p\u003e 7,5. Data PDC, tergantung pada hal (% vol.) diberikan dalam tabel. 1.6 (GOST 12.1.044-84). Tabel 1.6 Batas konsentrasi perambatan nyala (bawah dan atas) uap dan gas di udara Persamaan lain dikenal untuk menghitung CRPD, yaitu:
dimana C „dan Dari ke - dalam% (vol.); N adalah jumlah atom oksigen yang diperlukan untuk oksidasi penuh bahan bakar. Untuk bahan bakar C „N t
di mana C „- dalam% (vol.); () n - nilai kalor molar bersih, kJ / kmol. Untuk bahan bakar hidrokarbon SpN t pada 3 p 10, kesalahan perhitungan adalah ± 15%. Jika KPRP dikenal untuk komponen bahan bakar individual, maka KPRP yang lebih rendah direkomendasikan untuk dihitung dengan persamaan: di mana C dan C „adalah konsentrasi komponen pertama dalam campuran dan pada batas bawah,% (vol.). Untuk bahan bakar CpNt dalam pendekatan pertama a k ~ a p -1.42. Perhitungan ulang, dan C in in tapi n dan tapi n diproduksi oleh:  di mana С ("th") adalah konsentrasi bahan bakar di bagian bawah (atas) KPRP,% (vol.); MT dan Mo berat molekul bahan bakar dan zat pengoksidasi; L0 - dalam kg oksidator / kg bahan bakar; B m adalah koefisien stoikiometrik molar, mol okpellant / mol bahan bakar. Penghitungan ulang KPRP yang lebih rendah untuk berbagai suhu dapat dilakukan sesuai dengan persamaan: L II l T - 293 di mana Т „adalah suhu (dalam K) dari produk pembakaran campuran di mana konsentrasi bahan bakar pada 293 K sesuai dengan CRP yang lebih rendah (dalam perkiraan pertama, T„ untuk campuran udara hidrokarbon adalah 1600-1650K); С dan and adalah konsentrasi bahan bakar yang sesuai dengan batas konsentrasi yang lebih rendah pada suhu T dan 293 K, % (vol.). Persamaan (1,20) berlaku dalam kisaran suhu yang luas, namun tidak dapat digunakan pada suhu yang dekat dengan suhu penyalaan sendiri. Suhu produk pembakaran pada KPRP yang lebih rendah juga dapat dihitung dengan persamaan
stech dimana T „dalam K; T dengan suhu campuran sebelum pembakaran, K; Сссх - konsentrasi bahan bakar dalam campuran komposisi stoikiometrik,% (vol.); Srh adalah kapasitas panas isobarik rata-rata dari produk pembakaran pada suhu T, kJ / (kg ° C). CPRP praktis tidak tergantung pada ukuran bejana reaksi silinder, jika diameternya lebih dari 50 mm, dan untuk bola - jika volumenya melebihi 2000 cm 3. Untuk menentukan CRPD dan komposisi optimal campuran hidrokarbon-udara, grafik ditunjukkan pada Gambar. 1.26. C „, s,% (s)  Fig. 1.26. Batas konsentrasi perambatan nyala dalam campuran hidrokarbon-udara (St dan C ") dan konsentrasi hidrokarbon dalam campuran stoikiometrik (Cc,") tergantung pada koefisien stoikiometri molar 1 ^ m pada I20 ° C P \u003d 0,101 MPa:
Campuran yang mudah terbakar dari uap bahan bakar dengan udara di ruang bahan bakar hanya dapat terbentuk dalam kisaran suhu tertentu. Suhu minimum di mana campuran yang mudah terbakar masih dapat terbentuk dalam volume terbatas dari ruang bahan bakar, yang mampu terbakar stasioner ketika dinyalakan dari sumber eksternal, disebut batas suhu yang lebih rendah; itu sesuai dengan KPRP yang lebih rendah. Suhu tertinggi di mana campuran uap dengan udara di ruang bahan bakar masih mempertahankan kemampuan pembakaran stasioner disebut batas suhu atas; itu sesuai dengan KPRP atas. Penentuan eksperimental batas suhu untuk pembentukan campuran eksplosif dilakukan sesuai dengan GOST 12.1.044-89 (klausul 4.12), yang dihitung didasarkan pada penerapan standar yang sama. Suhu di mana batas suhu yang lebih rendah dari pembentukan campuran bahan peledak pada tekanan atmosfer tercapai, adalah kebiasaan untuk mengidentifikasi dengan titik nyala. Pada titik nyala, hanya campuran uap-udara yang dihasilkan terbakar, tetapi proses pembakarannya tidak stabil. Perhitungan batas suhu pembentukan campuran yang mudah terbakar dikurangi menjadi operasi berikut. Awalnya, pada tekanan total P yang diberikan dan diketahui nilai koefisien kelebihan oksidator (udara) yang sesuai dengan CPRP bawah dan atas (a n dan a c) dengan persamaan (1.22) tentukan tekanan parsial uap bahan bakar Rt: x | 0,232 o? 0 m t " ?« - di mana P adalah tekanan total, Pa; C - koefisien stoikiometri, kg oksidator / kg bahan bakar; a - koefisien zat pengoksidasi berlebih; Mt adalah massa mol bahan bakar, kg / kmol; Mo adalah massa mol zat pengoksidasi, untuk udara, Mo \u003d 28.966 kg / kmol; di/ 0 - konsentrasi oksigen dalam zat pengoksidasi berat.  Fig. 1.27. Kemudian, sesuai dengan tabel atau grafik Pts.p. \u003d ^ (0 (di mana P adalah tekanan uap jenuh bahan bakar), suhu yang sesuai dengan nilai-nilai yang dihitung dari Pt- ditemukan Jika batas konsentrasi untuk pembentukan campuran yang mudah terbakar tidak diketahui, maka batas suhu dapat dihitung dengan menggunakan persamaan: 1,15 1*(7,5 P d) - 0,239 3.31 di mana saya berada pada 0 C; 15% - suhu didih fraksi 5%, 0 С; RT adalah tekanan uap bahan bakar di CPRP (P „atau P„), kPa; 8 "c" adalah entropi penguapan pada suhu 15% dan tekanan atmosfer (diambil sesuai dengan jadwal pada Gambar. 1.28).  Fig. 1.28. 60 80 100 120 140 160 180 1, ° С Energi mudah terbakar dan batas konsentrasi pengapianSifat mudah-menyala dari campuran yang mudah terbakar homogen oleh sumber panas luar dicirikan oleh batas konsentrasi dan energi yang diperlukan untuk pengapiannya. Batas konsentrasi pengapian (CPV) disebut konsentrasi bahan bakar maksimum dalam campuran di mana sumber pengapian lokal (pelepasan listrik, benda panas, nyala api) mampu memastikan penyebaran proses pembakaran di seluruh volume campuran. Dengan analogi dengan KG1RP, CPV bawah dan atas dibedakan. Mereka tergantung pada sifat fisikokimia bahan bakar dan oksidator, energi dan jenis sumber pengapian, lokasinya, dll. Menurut Ya.B. Zeldovich, energi yang diperlukan untuk menyalakan campuran yang mudah terbakar homogen ditentukan: Y1-T dengan g (T 2 -T s) di mana pc dan T dengan - kepadatan dan suhu campuran; Tg - suhu produk pembakaran di zona pembakaran awal; L. 7 - koefisien konduktivitas termal dari produk pembakaran di Tg; dan „adalah kecepatan rambat api normal; C RT - medium kapasitas panas isobarik massa gas dalam lapisan bola 8 T yang mengelilingi zona pembakaran awal bola; 5, adalah lebar termal dari depan api. Persamaan (1,24) juga berlaku untuk kasus pengapian campuran bergerak jika konduktivitas termal L. 7 diganti dengan koefisien pertukaran turbulen IV / " (/ - skala turbulensi V / * adalah kecepatan denyut), dan nilai cn adalah kecepatan rambat nyala dalam aliran turbulen. Komposisi campuran sesuai dengan minimum kurva O \u003d COP,),disebut optimal. Untuk hidrokarbon parafin normal, konsentrasi bahan bakar dalam campuran komposisi optimal pada 25 ° C dapat ditentukan dari rasio:
Dengan meningkatkan konsentrasi oksigen dalam zat pengoksidasi, komposisi optimal campuran yang mudah terbakar bergeser ke wilayah konsentrasi bahan bakar yang lebih rendah. Ketergantungan energi pengapian optimal (minimum) pada tekanan dan suhu campuran yang mudah terbakar dijelaskan oleh persamaan [114]: O-opt   di mana Oopt adalah energi pengapian di P dan T, J; Cb adalah energi pengapian pada T \u003d 273 K dan P \u003d 10 5 Pa. Persamaan (1,26) memiliki korelasi yang baik dengan data eksperimen. Hubungan energi mudah terbakar optimal dengan konsentrasi oksigen dalam zat pengoksidasi dijelaskan oleh persamaan  di mana (С? 0 „„,) у / \u003d / adalah nilai optimal dari energi yang mudah terbakar dari campuran bahan bakar-oksigen; ~ konsentrasi volume oksigen dalam zat pengoksidasi; n adalah eksponen, dekat dengan kesatuan (n ~ 0.8). Data eksperimen untuk metana, etana, dan propana saat berubah c / x dari 0,1 hingga 0,21 dan tekanan dari 0,98 ke 19,6 kPa mengkonfirmasi persamaan (1,27). Tampaknya, itu tetap berlaku untuk campuran hidrokarbon. Konsentrasi bahan bakar dalam rentang pengapian dapat dihitung jika CRPD dan nilai-nilai () oph dan C opt diketahui oleh persamaan  o, 5 (s; + s;) \u003d С_ +0.15 (S. (1.29) Persamaan (1.28) dan (1.29) valid untuk - Mendenotasikan sisi kanan persamaan ini, masing-masing, B dan 0,5A, kita dapatkan C " - C " = B dan C " + C "\u003d A . (1.30) C "\u003d 0,5 (L-B) dan C; \u003d 0,5 (A + B). (1.31) Dalam persamaan di atas: C in dan C n - konsentrasi bahan bakar dalam campuran di CPRP atas dan bawah; C in dan C ", adalah konsentrasi bahan bakar dalam campuran di CPV atas dan bawah dengan energi yang mudah terbakar dari muatan listrik kapasitif; C opt adalah konsentrasi bahan bakar dalam campuran yang sesuai dengan O oph. Persamaan (1.28) dan (1.29) didasarkan pada hasil studi eksperimental yang ditunjukkan pada Gambar. 1.30.
 Fig. 1.30. Daerah penyalaan campuran C p N P1 + 02 + ^ tergantung pada energi yang mudah terbakar Batas konsentrasi pengapian tergantung pada kecepatan aliran, mendekati satu sama lain dengan peningkatannya (Gbr. 1.31 dan 1.32). Pengaruh kecepatan aliran pada energi pengapian dijelaskan dengan benar oleh persamaan: (2 \u003d (? O + Au "ke (1,32) di mana (Z0 adalah energi pengapian dari campuran stasioner, 10 "3 J; XV adalah kecepatan aliran, m / s; A adalah koefisien yang ditetapkan secara eksperimental.  Fig. 1.31.  Fig. 1.32. Koefisien udara berlebih dan campuran bensin-udara CPV tergantung pada laju aliran? dan tekanan P [114]: Titik nyala n suhu penyalaan otomatisTitik nyala adalah suhu minimum di mana campuran uap-udara yang dihasilkan dapat dinyalakan oleh sumber panas eksternal, tetapi proses pembakarannya tidak stabil. Titik nyala ditentukan secara eksperimental dalam wadah terbuka atau tertutup sesuai dengan GOST 12.1.044-84 (pasal 4.3 dan 4.4). Perhitungan titik nyala dibuat sesuai dengan GOST 12.1.044.84 (paragraf 4.5). Titik nyala adalah 10-15 ° C di bawah batas suhu untuk pembentukan campuran yang mudah terbakar yang mampu merambat nyala api. Untuk perkiraan perkiraan suhu blitz, seseorang dapat menggunakan ketergantungan yang disajikan pada Gambar. 1.33.  Fig. 1.33. Titik nyala 1 V cc bahan bakar jet dan bensin B-70 tergantung pada tekanan uap jenuh Pn pada 1 \u003d 40 ° C dalam wadah tertutup (62): o - bahan bakar dengan komposisi berbeda; - kurva umum Penyalaan sendiri adalah proses penyalaan campuran yang mudah terbakar tanpa kontak dengan nyala api atau benda panas. Suhu awal minimum yang memadai untuk penyalaan otomatis campuran yang mudah terbakar disebut suhu penyalaan otomatis. Itu tergantung pada sifat kimiawi bahan bakar, komposisi campuran udara-bahan bakar, tekanan, adiabatik dari proses penyalaan sendiri, adanya katalis dan penghambat oksidasi dan faktor-faktor lainnya. Interval waktu antara saat campuran yang mudah terbakar mencapai suhu penyalaan sendiri dan penampilan nyala disebut periode penundaan penyalaan diri. Ketika memasok bahan bakar cair, itu mencakup proses atomisasi, pemanasan dan penguapan tetesan bahan bakar, difusi uap bahan bakar dan oksigen dan, akhirnya, reaksi kimia. Suhu dan waktu tunda penyalaan sendiri terkait dengan rasio:  dimana E - energi aktivasi yang efektif, kJ / kmol; E \u003d 8.31419 kJ / (kmol K) adalah konstanta gas universal; t - periode tunda penyalaan sendiri pada suhu T. Kecenderungan hidrokarbon dan campurannya untuk penyalaan sendiri ditandai oleh suhu minimum penyalaan sendiri yang diperoleh di bawah kondisi adiabatik, ketika durasi paparan campuran yang mudah terbakar di bawah kondisi awal yang diberikan tidak membatasi proses penyalaan sendiri. Suhu penyalaan otomatis minimum ditentukan secara unik oleh struktur molekul. Jadi, misalnya, untuk hidrokarbon parafin, 1 sv berhubungan langsung dengan panjang efektif rantai karbon bc, yang dihitung dengan persamaan:
di mana g adalah jumlah gugus CH 3 dalam molekul; k adalah jumlah rantai karbon yang dimulai dan diakhiri dengan gugus CH 3; m * adalah jumlah rantai yang mungkin mengandung atom karbon ^. Ketergantungan 1 b \u003d A (bc) ditunjukkan pada Gambar. 1.34.  Fig. 1.34.
Suhu penyalaan otomatis campuran hidrokarbon tidak mematuhi aturan aditivitas, biasanya lebih rendah dari yang dihitung berdasarkan aturan ini. Data pada suhu penyalaan otomatis campuran bahan bakar udara dari komposisi optimal tergantung pada jumlah atom karbon dalam molekul hidrokarbon (untuk bahan bakar jet dalam formula di atas) disajikan pada Gambar. 1.35. Efek tekanan dan konsentrasi oksigen dalam zat pengoksidasi diilustrasikan oleh data yang ditunjukkan pada Gambar. 1.36.  Fig. 1.35. Ketergantungan suhu penyalaan otomatis campuran bahan bakar udara dari komposisi optimal pada jumlah atom hidrokarbon n dalam molekul pada P \u003d 0,101 MPa [124]; t adalah periode tunda autoignition; t L - "o; R.T. - bahan bakar jet (p-dalam rumus di atas) - parafin; a-olefin; ? - hidrokarbon naftenat  Fig. 1.36. Ketergantungan suhu penyalaan otomatis bahan bakar T-6 pada tekanan P dan konsentrasi oksigen dalam zat pengoksidasi f 0 2 (menurut V.V. Malyshev): 2 = 0 2 / (° 2 + L, g) Temperatur penyalaan otomatis ditentukan oleh kemampuan bahan bakar untuk membentuk campuran yang mudah terbakar dalam fase uap. Oleh karena itu suhu self-ignition dari suspensi adalah bahan bakar ditentukan oleh media dispersi dan pengental. Fase terdispersi mengambil bagian dalam proses penyalaan sendiri hanya di bagian penyerapan panas ketika suspensi dipanaskan hingga suhu penyalaan otomatis dari fase cair. Tekanan LedakanTekanan ledakan adalah tekanan tertinggi yang terjadi selama ledakan deflagrasi campuran uap-udara dalam volume tertutup pada tekanan awal 0,101 MPa. Tingkat kenaikan tekanan ledakan - turunan waktu dari tekanan ledakan (s1P / (1t) di bagian naik ketergantungan P \u003d Y t). Secara eksperimental, tekanan ledakan maksimum dan laju peningkatan tekanan selama ledakan campuran uap-udara ditentukan sesuai dengan GOST 12.1.044-89 (Lampiran 8). Perhitungan laju peningkatan tekanan selama ledakan dilakukan sesuai dengan GOST 12.1.044-89 (Lampiran 12). Tekanan ledakan ditentukan oleh:  di mana Rvzr - tekanan ledakan, Pa; P „adalah tekanan awal, Pa; T „, dan T ps - suhu awal dan suhu produk pembakaran. K; spike adalah jumlah mol produk pembakaran dan campuran umpan. Tingkat kenaikan tekanan maksimum (dalam Pa / s) dihitung oleh persamaan  di mana Po adalah tekanan awal. Pa; dan „adalah kecepatan rambat api normal pada Po dan To m / s; Itu adalah suhu awal campuran, K; g adalah jari-jari bom, m; n - P m / P 0 - mengurangi tekanan ledakan maksimum; K adalah indeks adiabatik untuk campuran uji; e - indikator termokinetik, tergantung pada dan n, tekanan dan suhu; jika nilainya e tidak diketahui, diambil sama dengan 0,4. Tingkat rata-rata kenaikan tekanan (dalam Pa / s) dihitung dengan persamaan: "s1P _ ZR 0 dan ‘(i -) - i k * e ^ m) dengan y / (l, k, e) dimana ^ tg, k 7 e) -fungsi, nilainya ditemukan oleh gambar nomogram. 1.37.  Fig. 1.37. Ketergantungan fungsi / (n, c.c) dari tekanan yang berkurang n \u003d P / PK,indeks adiabatik untuk dan indikator termokinetik dengan campuran uji (Lampiran untuk GOST 12.1.044-84) Nilai-nilai tg dan k ditemukan dengan perhitungan termodinamika atau. dalam hal ketidakmungkinan perhitungan, terima untuk \u003d 9.0 dan k \u003d 1.4. Situasi darurat dan daruratKecelakaan - kecelakaan industri berbahaya yang menciptakan ancaman terhadap kehidupan dan kesehatan orang-orang di fasilitas, wilayah atau wilayah air tertentu dan mengarah pada penghancuran bangunan, struktur, peralatan dan kendaraan, gangguan proses produksi atau transportasi, serta kerusakan lingkungan (GOST R 22.0 .05-94). Kecelakaan adalah pelepasan energi destruktif yang tidak terkendali atau komponen aktif secara kimiawi (secara biologis, radiasi). Bergantung pada sumber kejadiannya, situasi darurat (ES) yang bersifat alami, teknogenik dan alami-teknogenik dibedakan. Dalam gbr. 1.38 menunjukkan peningkatan relatif dalam jumlah kecelakaan dan bencana alam, teknologi, dan teknologi alam di Rusia. Dalam gbr. 1,39 menyajikan dinamika jumlah semua kecelakaan teknologi di Rusia untuk periode 1990-94. Gambar tersebut menunjukkan bahwa peningkatan jumlah keadaan darurat tidak terjadi dengan lancar, tetapi secara spasmodik, dengan lonjakan terjadi segera setelah pergolakan sosial (Agustus 1991, Oktober 1993). Jumlah darurat buatan manusia telah meningkat secara tajam dalam beberapa tahun terakhir, termasuk dalam penerbangan. Obyek potensial dari kecelakaan adalah pesawat terbang, serta penyimpanan dan gudang produk minyak yang mudah meledak dan kebakaran yang terletak di bandara, titik pengisian bahan bakar dan pemeliharaan, dan titik perbaikan. Penyebab situasi darurat mungkin tumpahan minyak. produk melalui unit penyegelan katup penutup, pompa transfer, saluran pipa dan perangkat pengisian cairan; melalui ventilasi ruang gas tangki; meluapnya tangki, tangki dan tangki; pembersihan tangki; penghancuran korosi reservoir dan komunikasi. Berbagai kontainer dioperasikan untuk penyimpanan dan transportasi produk minyak bumi. Keamanan pengoperasian wadah ditentukan oleh kekuatan yang disediakan. Namun, kecelakaan di fasilitas tersebut dapat terjadi karena kekurangan dalam sistem yang ada untuk memantau dan memantau keadaan struktur, serta kurangnya dokumentasi peraturan dan teknis. Keamanan pengoperasian fasilitas penyimpanan produk minyak harus dipastikan selama desain, konstruksi, dan operasi. Pendekatan ini ditentukan oleh analisis penerimaan dan dokumentasi operasional, serta penyebab situasi darurat. Tugas penting, solusi yang akan meningkatkan keandalan fasilitas penyimpanan operasi, adalah untuk melakukan survei teknis komprehensif berbasis ilmiah dan melengkapi sistem pemantauan diagnostik dan operasional untuk kondisi logam, pondasi, struktur isolasi panas, dan peralatan teknologi. Untuk manajemen aliran produk minyak yang aman, kemudahan kerja katup proses pipa: shut-off, throttle, alat pengaman sangat penting; katup kontrol; alat kelengkapan kerja terbalik (untuk mencegah kemungkinan perpindahan produk yang berlawanan dengan pekerja); katup darurat dan penutup (untuk memblokir aliran secara otomatis ke bagian darurat atau penutupannya), drainase kondensat, dll. Jumlah kecelakaan  Fig. 1.38.
 Fig. 1.39. Ketika peralatan ditekan, produk akan kedaluwarsa dan menguap dengan cepat dengan pembentukan campuran gas-udara berbahaya yang bisa meledak dan berbahaya. Pelepasan atau kebocoran campuran gas-uap yang tidak disengaja menyebabkan pembentukan awan yang dapat meledak. Peledakan dari siklus gabungan dan sistem aerodispersi dipertimbangkan dalam pekerjaan ini. Terjadinya ledakan di awan besar dijelaskan oleh mekanisme berikut. Yang pertama dari mereka memperhitungkan kemungkinan tindakan radiasi termal yang intens dari api panjang di awan yang sebelumnya dicampur oleh aliran gas turbulen. Mekanisme kedua untuk terjadinya peledakan melibatkan percepatan api di awan besar karena perbedaan dalam percepatan volume elementer gas yang terbakar dan campuran segar dalam nyala yang bergejolak. Perbedaan ini muncul di bawah pengaruh gradien tekanan rata-rata dalam nyala api karena daya apung yang berbeda dari volume gas yang berbeda, yang mengarah ke turbulisasi tambahan aliran dan munculnya umpan balik. Mekanisme umpan balik positif ini, yang ditentukan oleh perbedaan kepadatan di berbagai zona awan, dapat secara signifikan mengintensifkan percepatan api. Pengapian disertai dengan lampu kilat suhu tinggi yang cerah. Sosok geometris yang paling dapat diterima dari campuran uap-gas yang terlintas adalah sosok bola yang tidak beraturan atau elips (bola api). Dengan bola api (OS) berarti produk dari penguapan tiba-tiba atau kebocoran bahan bakar gas (atau gas), disertai dengan wabah mereka dan pembakaran normal atau deflagration berikutnya. Untuk banyak bahan bakar hidrokarbon dari pelepasan linier dan siklik dalam kisaran kepadatan 700 hingga 1000 kg / m 3, rasio diameter bola api diberikan: di mana M adalah massa bahan bakar dalam OSH, kg.; TF - suhu aktual di OR (di awan), 0 С; Trep - referensi (referensi) suhu, ° С. Kisaran koefisien 4.2n-5.3 tergantung pada jenis bahan bakar dan kondisi pembentukan awan. Untuk masa pakai awan selama pembakaran alami, ekspresi memiliki bentuk: m \u003d 0M- * 1m-1 ±. Ketergantungan ini ditunjukkan pada Gambar. 1.40 dan 1.41.  Fig. 1.40.  Fig. 1.41. Ada bahaya besar ledakan campuran uap-gas dalam volume tertutup. Di atas meja. 1.7 menunjukkan batas-batas ledakan hidrokarbon di udara dalam volume tertutup dan ruang terbuka, yang menunjukkan risiko lebih besar dari ledakan campuran gas atau uap-gas dalam volume tertutup. Ini dijelaskan baik oleh proses percepatan reaksi karena peningkatan autokatalisis, dan karena amplifikasi gelombang yang dipantulkan ketika proses b-ary telah dimulai, dan karena sejumlah alasan kinetik yang selalu ada. Meningkatnya kemudahan eksitasi peledakan dalam kapal disebabkan oleh kemampuan dinding untuk menghasilkan turbulensi dalam aliran di depan nyala api, yang mempercepat transisi pembakaran menjadi detonasi. Batas detonasi hidrokarbon di udara Ledakan campuran gas yang terakumulasi dapat terjadi di bawah pengaruh percikan acak. Dengan pemuatan terbuka produk minyak, ledakan akibat pelepasan statis juga dimungkinkan, khususnya, karena tidak ada perangkat pengardean. Penyebab paling umum ledakan adalah percikan, termasuk sebagai akibat dari akumulasi listrik statis. Percikan listrik dapat terjadi tanpa konduktor atau jaringan sama sekali. Ini berbahaya karena terjadi di tempat-tempat yang paling tidak terduga: di dinding tank, di ban mobil, di baju, di benturan, selama gesekan, dll. Penyebab lain ledakan adalah kelalaian dan ketidakdisiplinan pekerja. Jika pembentukan campuran uap-gas dimungkinkan, perlu untuk memastikan proteksi petir yang andal, perlindungan terhadap listrik statis, memberikan langkah-langkah terhadap percikan peralatan listrik dan peralatan lainnya. Dalam kecelakaan yang melibatkan ledakan, perusakan benda-benda di sekitarnya terjadi dan orang-orang terluka. Penghancuran adalah hasil dari tindakan prismatik produk ledakan dan gelombang kejut udara. Dalam hal ini, faktor-faktor kerusakan utama adalah gelombang kejut, radiasi termal-cahaya dan beban racun (karbon monoksida). Orang dengan jarak 5 m menerima luka bakar tingkat 1 dan lesi lainnya. Kecelakaan terkait ledakan sering kali disertai dengan kebakaran, yang dapat menyebabkan konsekuensi bencana dan ledakan selanjutnya yang lebih kuat dan kerusakan yang lebih parah. Penyebab kebakaran biasanya sama dengan ledakan. Selain itu, ledakan dapat menjadi penyebab atau efek dari api, dan sebaliknya, api dapat menjadi penyebab atau efek dari ledakan. Api adalah generasi yang berkembang secara spontan yang tidak disediakan oleh proses teknologi. Pembakaran produk minyak bumi dapat terjadi dalam tangki, peralatan industri dan selama tumpahan di area terbuka. Jika terjadi kebakaran produk minyak di dalam tangki, ledakan, pendidihan dan pelepasannya dapat terjadi, dan akibatnya, tumpahan cairan panas. Bahaya besar adalah emisi dan pendidihan produk minyak bumi, yang terkait dengan keberadaan air di dalamnya, dan ditandai dengan pembakaran yang cepat dari massa produk berbusa. Saat mendidih, suhu meningkat tajam (hingga 1500 ° C) dan tinggi nyala api. Untuk menilai tingkat kerusakan pada suatu objek, apa yang disebut kurva ambang biasanya digunakan yang menghubungkan fluks energi panas-cahaya q (fluks panas) dan energi total insiden O pada unit permukaan (Gbr. 1.42).  Fig. 1.42. Dengan waktu paparan termal yang besar, melebihi waktu dari kemungkinan keberadaan objek yang tidak terganggu, ambang kerusakan akan ditentukan secara eksklusif oleh fluks termal (cahaya termal) I. Di bawah efek berdenyut dari paparan singkat, ambang akan ditentukan terutama oleh energi O. Nilai I dan O melebihi ambang akan menyebabkan kerusakan tanpa syarat pada objek. Jika I atau O kurang dari nilai ambangnya, maka lesi tipikal tidak ada dan hanya sedikit ketidaknyamanan yang mungkin terjadi. Sebagai contoh, dengan peningkatan durasi radiasi dari 0,5 menjadi 2 detik, saya berkurang dari 120 menjadi 30 unit, yaitu dengan sedikit peningkatan O, bahkan dengan peningkatan waktu paparan sebanyak 4 kali, merusak cedera tidak ada, dan seseorang hanya dapat merasakan ketidaknyamanan ringan. Namun, nilai total insiden energi O pada target, dalam periode waktu yang sama tumbuh dari sekitar 10 hingga 25 unit. (^. Dengan demikian, garis K, yang menanggapi perubahan I dan O yang saling berhubungan, membentuk zona (wilayah) lesi, yang ditunjukkan pada gambar di sebelah kanan garis K. Salah satu konsekuensi paling tidak menyenangkan dari kekalahan energi radiasi adalah luka bakar "tongkat" dan "kerucut" mata. Dalam gbr. 1,43, ketergantungan i pada m, serta T pada m, diberikan, yang menentukan area nyeri toleran dan tidak toleran selama pembentukan luka bakar termal dengan derajat yang berbeda-beda. Kriteria yang diterapkan pada gambar yang disajikan didasarkan pada kenyataan bahwa rasa sakit yang tak tertahankan terjadi selama iradiasi termal ketika suhu lapisan kulit dengan ketebalan sekitar 0,14-0,15 mm (di bawah permukaan lapisan epitel atas) mencapai atau melebihi suhu 45 ° C. Setelah menghilangkan radiasi (tetapi tidak lebih dari 20-30 detik), rasa sakit yang tajam mereda, dan kemudian, sebagai aturan, menghilang sama sekali. Peningkatan suhu lapisan yang ditentukan oleh 4-10 derajat atau lebih menyebabkan rasa sakit dan kulit terbakar. Area nyeri yang dapat ditoleransi yang ditunjukkan dalam grafik ditentukan oleh fakta bahwa pada saat terpapar radiasi, refleks pelindung biologis muncul, menyebabkan peningkatan aliran darah dari area perifer tubuh, yang mencegah kenaikan suhu lokal ke tingkat ambang batas. Ketika terkena tekanan termal dosis tinggi, mekanisme fisiologis ini tidak lagi dapat menyediakan heat sink yang diperlukan, dan tubuh mengalami patologis, dan kadang-kadang beban panas transendental. Dari sifat garis pada Gambar. 1,42 dapat dilihat bahwa ada kuantitatif tertentu dosis radiasi q dan suhu T, yang menyebabkan kerusakan termal dan munculnya rasa sakit yang tak tertahankan sambil memberikan dosis ini dengan waktu pemaparan yang diperlukan. Durasi paparan, s Gambar 1.43. Batas panas dan cahaya Kecelakaan dengan pesawat terbang (LA) terjadi terutama karena unit yang tidak berfungsi, di tempat pertama - kegagalan mesin, serangan teroris, kebakaran, dan disertai dengan ledakan. Sebuah ledakan dapat terjadi di udara atau ketika menyentuh tanah. Ketika pesawat jatuh ke daerah perumahan, orang-orang, struktur, dll dapat menderita Contoh-contoh situasi darurat penerbangan, analisis mereka diberikan dalam karya. Salah satu bahaya utama dalam penerbangan adalah kemungkinan kebakaran selama pendaratan darurat. Bahan bakar yang berasal dari tangki yang rusak dapat terbakar dari percikan yang disebabkan oleh gesekan, dari panas permukaan atau api terbuka. Dalam hal ini, zona pembakaran yang dihasilkan dengan cepat menyebar di semua zona di mana nilai rasio udara uap / bahan bakar berada dalam kisaran mudah terbakar. Salah satu metode untuk mengurangi risiko kebakaran adalah dengan menggunakan bahan bakar kental, yang menyebar lebih lambat dan memiliki volatilitas lebih rendah daripada bahan bakar cair konvensional. Jika tangki dengan bahan bakar menebal rusak, laju penyebaran bahan bakar dan laju pembentukan aerosol yang mudah terbakar menurun tajam. Ini memungkinkan Anda untuk meningkatkan periode waktu di mana penumpang dapat dievakuasi. Keadaan darurat dan situasi darurat menyebabkan kerusakan material yang parah dan memperburuk masalah lingkungan. Dalam kecelakaan yang disertai dengan ledakan dan kebakaran, ada dampak mekanis, termal, dan kimia yang kuat pada lingkungan sekitar. Pada saat yang sama, emisi polutan meningkat tajam; permukaan bumi tersumbat oleh puing LL, residu bahan bakar, produk pembakaran; kerusakan signifikan pada bentang alam, flora, fauna; padang rumput, tanah subur mati. Efek mekanis ditandai dengan pelanggaran lapisan tanah atas (subur) karena semua kerusakan permukaan dan dalam, dampak energi ledakan (gelombang kejut); pelanggaran tutupan rumput, kerusakan atau kematian semak, pohon dan vegetasi lainnya. Struktur lapisan subur atas, pertukaran gas dan air, struktur kapiler berubah. Tindakan yang ditujukan untuk meningkatkan keselamatan dalam situasi darurat biasanya dibagi menjadi dua kategori. Yang pertama termasuk acara yang diadakan setelah situasi darurat. Peristiwa El1 biasanya disebut operasional, dan pada dasarnya dikurangi untuk melindungi populasi dan menghilangkan konsekuensi dari keadaan darurat. Kelompok tindakan kedua mencakup kegiatan yang dilakukan sebelumnya. Ini termasuk meningkatkan keandalan peralatan teknologi, mengurangi timbunan zat berbahaya di fasilitas, menghilangkan fasilitas berbahaya, dan langkah-langkah awal untuk melindungi orang. Sistem keselamatan penerbangan aktif (ASOBP) penting, yang merupakan elemen dari sistem pendukung pilot "cerdas" di atas kapal, yang dikenal dalam praktik penerbangan sebagai "asisten pilot", yang dirancang untuk beroperasi dalam situasi reguler dan darurat. ASOBP memberikan sinyal peringatan tentang ancaman terhadap keselamatan penerbangan, serta segera memberi informasi dalam bentuk "tips" tentang manajemen pesawat dan kompleknya di udara untuk mencegah LA mencapai kondisi penerbangan yang kritis. Untuk mencegah tabrakan dengan permukaan bumi dan di antara pesawat, ASOBP membentuk lintasan spasial "berkembang biak". Salah satu bidang pencegahan kecelakaan yang paling efektif adalah investigasi yang lengkap, mendalam dan obyektif atas peristiwa masa lalu dan pengembangan atas dasar rekomendasi ini untuk mencegah terulangnya kejadian tersebut. Efektivitas kerja semacam itu tidak hanya bergantung pada tingkat sumber daya yang memadai, tetapi juga pada kekuatan menyeluruh dari badan yang melakukan penyelidikan independen, yang memungkinkan untuk mempengaruhi area sistem transportasi udara (produksi, desain, pengujian, sertifikasi, operasi, perbaikan, kerangka kerja regulasi, dll.) . Standar 5.4. Lampiran 13 pada Konvensi Penerbangan Sipil Internasional menyatakan: "Otoritas untuk investigasi kecelakaan harus diberikan independensi untuk melakukan penyelidikan dan otoritas tidak terbatas untuk melakukan itu". Persyaratan ini juga diterapkan dalam Peraturan Investigasi Rusia, yang disetujui oleh Pemerintah Federasi Rusia. Komite Penerbangan Antar Negara (IAC) yang dibentuk oleh Perjanjian menerima dari kepala negara dan pemerintah CIS hak untuk secara independen menyelidiki kecelakaan pesawat. Sejak 1992, para ahli IAC telah menyelidiki lebih dari 270 kecelakaan pesawat, termasuk lebih dari 50 kecelakaan internasional, termasuk investigasi terhadap peristiwa yang melibatkan pesawat buatan Barat. Saat ini ada tujuh pusat investigasi kecelakaan khusus di dunia (AS, Prancis, Inggris, Kanada, Jerman, Australia, dan IAC). Yang tidak kalah pentingnya adalah penyediaan informasi dari negara-negara bagian dengan data tentang kegagalan dan malfungsi pesawat dan tindakan kru yang salah. Dengan menggunakan data ini, otoritas penerbangan dari masing-masing negara bagian dapat mengambil tindakan pencegahan. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Gbr. 7. Depan pembakaran bunsen depan
Dengan posisi stabil dari depan pembakaran, kecepatan rambat nyala api diimbangi oleh komponen W n normal ke permukaan kerucut pembakaran, kecepatan campuran gas-udara W, mis.
di mana j adalah sudut antara vektor kecepatan campuran gas-udara dan vektor komponennya yang normal ke permukaan kerucut pembakaran.
Nilai kecepatan campuran gas-udara di pintu keluar nozzle dengan kerucut pembakaran dari bentuk yang benar ditentukan oleh rumus
di mana d 0 adalah diameter nozzle burner, V adalah laju aliran campuran gas-udara melalui burner.
Nilai cos j dapat dinyatakan dalam hal ketinggian kerucut pembakaran
Mengingat bahwa permukaan pembakaran adalah permukaan sisi kerucut biasa
nilai kecepatan normal ditentukan
Kecepatan rambat api normal dipengaruhi oleh:
1. Suhu awal campuran. Pada suhu rendah, biasanya berbanding lurus dengan kuadrat dari suhu absolut campuran yang memasuki pembakaran. Pada suhu yang melebihi suhu penyalaan, konsep kecepatan normal kehilangan maknanya, karena campuran menjadi mampu menyala sendiri.
2. Suhu dinding saluran, asalkan nyala merambat di dalam saluran ini. Dinding dingin mengganggu reaksi berantai dan menghambat perambatan nyala api.
3. Diameter saluran. Untuk setiap campuran yang mudah terbakar ada nilai kritis diameter d cr, mulai dari mana perambatan api di dalam saluran tidak mungkin. Nilai diameter kritis dapat ditentukan oleh rumus
di mana cm adalah koefisien difusi termal campuran.
4. Tekanan. Dengan meningkatnya tekanan, maka berkurang.
5. Komposisi campuran. Untuk campuran dengan komposisi yang mendekati stoikiometrik, kecepatan normal memiliki nilai maksimum. Selain itu, ada batas bawah dan atas pada konsentrasi bahan bakar di luar yang nyala tidak dapat merambat.
Baru
- Mengisi bahan bakar mobil dengan HBO: bagaimana cara mengisi bahan bakar dengan benar dan aman?
- Bagaimana bantalan mixer beton diganti? Haruskah ada permainan pada mixer beton
- Gantungan kunci tanah liat. Gantungan kunci dinding. Kelas master Langkah-langkah kelas master: penjaga do-it-yourself
- Pilihan murah untuk kelongsong eksternal untuk menyelesaikan rumah kayu
- Cara melindungi garasi beton dengan tangan Anda sendiri
- Pasokan panas dan pemanas gedung bertingkat. Pemanas otonom dari gedung bertingkat
- Bagaimana dan apa yang harus melindungi lantai beton di rumah pribadi dengan tangan Anda sendiri dengan benar
- Pemanasan matahari di rumah pribadi Pemanasan di rumah pribadi dari matahari
- Pemanasan DIY dari rumah pribadi dua lantai - skema
- Penoizol: ulasan, spesifikasi



 - Zona pembakaran laminar;
- Zona pembakaran laminar;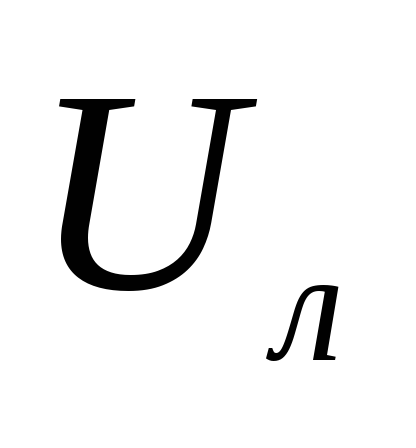 –– laju pembakaran laminar.
–– laju pembakaran laminar.
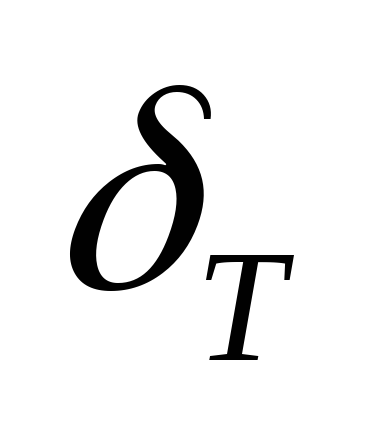 –– zona pembakaran turbulen;
–– zona pembakaran turbulen;
 –Kecepatan normal partikel kecil.
–Kecepatan normal partikel kecil.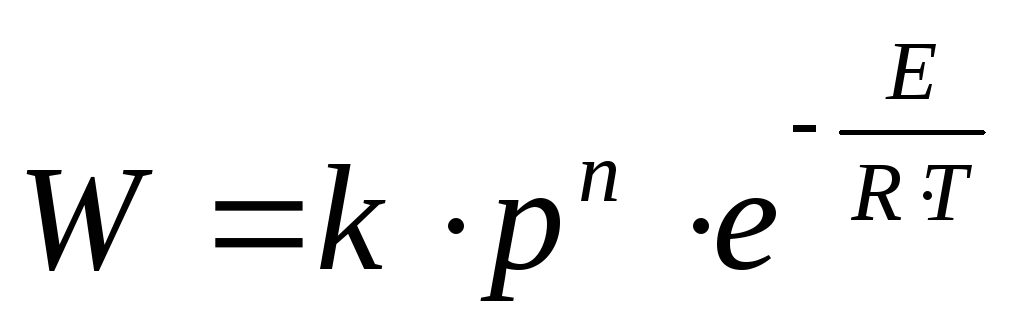 - laju reaksi kimia.
- laju reaksi kimia.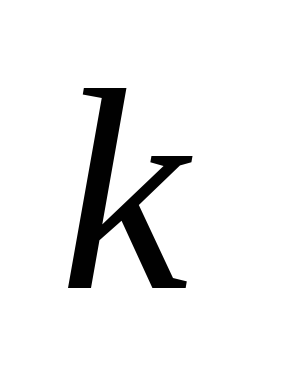 –Bahan konstan dari reaksi kimia, tergantung pada komposisi campuran dan jenis bahan bakar;
–Bahan konstan dari reaksi kimia, tergantung pada komposisi campuran dan jenis bahan bakar; –Tekanan dari reaksi kimia;
–Tekanan dari reaksi kimia; –Order reaksi kimia;
–Order reaksi kimia; 
 - Konstanta gas universal;
- Konstanta gas universal; - Suhu reaksi kimia;
- Suhu reaksi kimia; - Energi aktivasi adalah energi yang dibutuhkan untuk memutus ikatan intramolekul.
- Energi aktivasi adalah energi yang dibutuhkan untuk memutus ikatan intramolekul.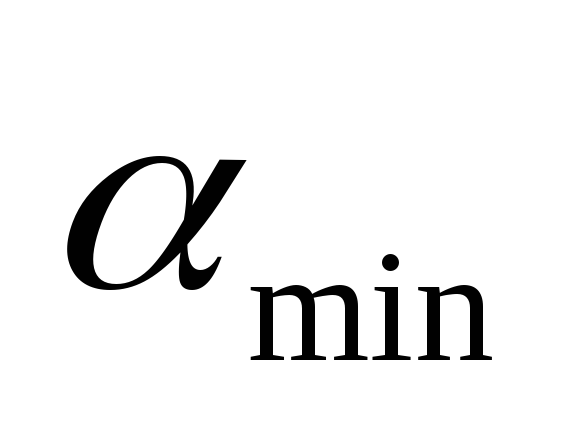
 –– batas konsentrasi atas;
–– batas konsentrasi atas; - Batas konsentrasi rendah;
- Batas konsentrasi rendah; - Pembakaran normal;
- Pembakaran normal;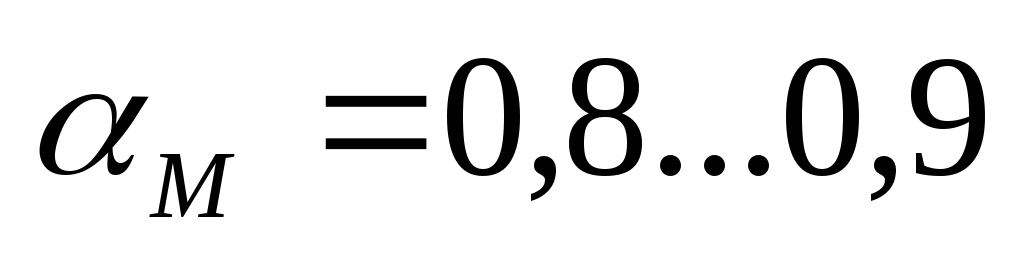
 –komposisi kekuatan campuran
- tenaga maksimum yang dikembangkan oleh mesin.
–komposisi kekuatan campuran
- tenaga maksimum yang dikembangkan oleh mesin.
 –komposisi ekonomi dari campuran
- profitabilitas maksimum.
–komposisi ekonomi dari campuran
- profitabilitas maksimum.

 membutuhkan penyesuaian waktu pengapian (SPD).
membutuhkan penyesuaian waktu pengapian (SPD).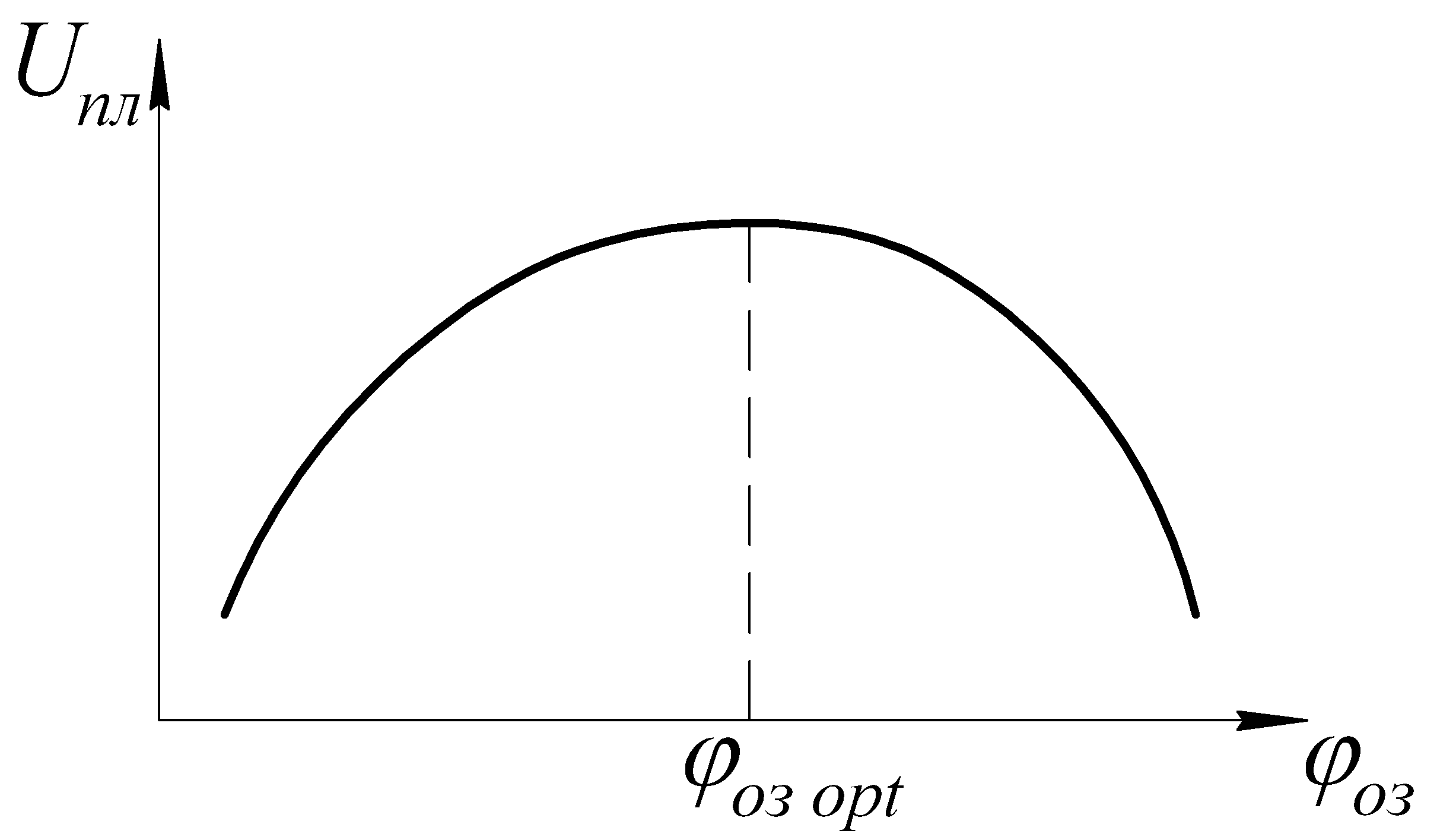
 beban od
memahami sudut rotasi throttle - dialah yang mengatur beban pada mesin.
beban od
memahami sudut rotasi throttle - dialah yang mengatur beban pada mesin.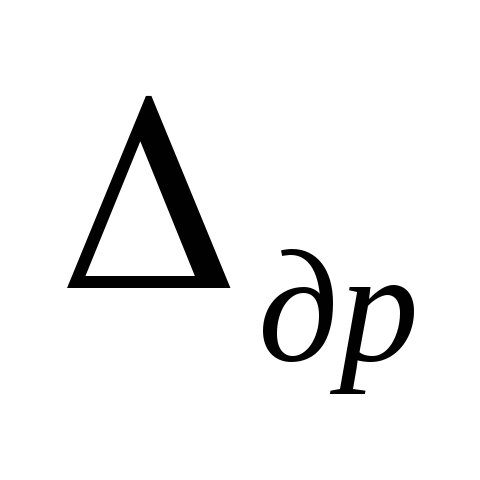 –Trik sudut rotasi.
–Trik sudut rotasi. nada
- pembakaran campuran yang eksplosif, disertai dengan gelombang kejut tekanan yang merambat di seluruh volume ruang pembakaran. Detonasi terjadi sebagai akibat dari penyalaan sendiri bagian campuran yang jauh dari lilin karena pemanasan yang kuat dan kompresi selama perambatan bagian depan nyala api.
nada
- pembakaran campuran yang eksplosif, disertai dengan gelombang kejut tekanan yang merambat di seluruh volume ruang pembakaran. Detonasi terjadi sebagai akibat dari penyalaan sendiri bagian campuran yang jauh dari lilin karena pemanasan yang kuat dan kompresi selama perambatan bagian depan nyala api.

 kami mencantumkan faktor-faktor yang menyebabkan peledakan:
kami mencantumkan faktor-faktor yang menyebabkan peledakan:
 - bensin mobil;
- bensin mobil;